In den letzten zehn Jahren haben neue Verfahren zur Aufbereitung von Blutbestandteilen zur Injektionstherapie am Bewegungsapparat einen regelrechten Boom erlebt. Es haben sich viele verschiedene Verfahren, Bezeichnungen, Anbieter und Techniken am Markt etabliert. Daher ist es nicht nur für den Praktiker schwer geworden, den Überblick zu behalten. Auch in der Literatur ist es mittlerweile bei vielen Publikationen fast unmöglich geworden, einwandfrei festzustellen, mit welchem Präparat und welcher Herstellungsweise bestimmte Studien durchgeführt wurden.
Alleine unter der Überbezeichnung PRP (Platelet Rich Plasma), der wohl bekanntesten Anwendungsform, verbergen sich zahlreiche Untergruppen, die sich z. B. durch die Anzahl, Länge und Geschwindigkeit der Zentrifugation(en), den zugesetzten Inhaltsstoffen und der Art der Auftrennung bzw. Abpipettierung und damit in der Zusammensetzung zum Teil deutlich unterscheiden.
Uneinheitliche Datenlage
Leider ist die Datenlage für fast alle diese Verfahren zum einen sehr uneinheitlich und generell meist zu gering, um sie alleine vom wissenschaftlichen Standpunkt aus für ihren Einsatz im Breiten- und Leistungssport zu bewerten. Zwar gibt es, wie z. B. zum PRP, mittlerweile eine erhebliche Anzahl von Veröffentlichungen, leider sind die überwiegende Mehrzahl aber mit wenigen Ausnahmen von minderer Qualität und verfügen meist über zu geringe Probandenzahlen (oft nur 20 – 30 Patienten insgesamt), um sichere und allgemeingültige Aussagen treffen zu können. Zudem sind die vorliegenden Ergebnisse sehr uneinheitlich, was zum einen daran liegt, dass es weltweit über 40 etablierte Verfahren und Systeme zur Herstellung von PRP gibt und viele Studien mit unterschiedlichen Verfahren durchgeführt wurden. Während fast alle in Deutschland marktüblichen Verfahren zur PRP-Herstellung nur einen Zentrifugationsschritt vorsehen, beinhalten die meisten Studien aus dem angloamerikanischen Sprachraum Verfahren mit zwei Zentrifgationsschritten, was die Vergleichbarkeit deutlich herabsetzt. Oft ist dem Studiendesign vieler, gerade älterer Studien, nicht einmal zu entnehmen, um welche Herstellungsweise es sich bei dem verwendeten PRP überhaupt gehandelt hat. Hier müssen wir uns nach wie vor neben den ersten Ergebnissen der Grundlagen- und klinischen Forschung auf die eigenen Erfahrungswerte, den seriösen Austausch mit erfahrenen Kollegen und nicht zuletzt auf die Rückmeldungen unserer Athleten verlassen. Die Sportmedizin ist und bleibt eine Erfahrungswissenschaft, bedarf aber einer individuell optimierten Behandlung eines jeden Athleten. Trotzdem ist es völlig ohne Evidenzbasis aber schwierig, aus den vielen Angeboten und Heilsversprechungen die seriösen, sicheren und nachweislich wirksamen Verfahren zu identifizieren. So liegt mittlerweile z. B. zur Behandlung der Gonarthrose mit Blutserum-Präparaten eine gute und sehr konsistente Datenlage mit mehreren Level I-Studien (Ramdomized Controlled Trials, RCTs) vor, die die Wirksamkeit belegen. Zum Einsatz bei Muskel- und Sehnenverletzungen mehren sich die Studien mit positiven Ergebnissen ebenfalls, jedoch mit deutlich heterogeneren Ergebnissen. Daher lohnt es sich, diese sehr populäre und häufig eingesetzte Produktklasse einmal näher zu betrachten und sich die Systematik ihrer Einteilung hinsichtlich Herstellung, Zusammensetzung und Erkenntnisse zur angenommenen Wirkweise klar zu machen.
PRP (Platelet Rich Plasma)
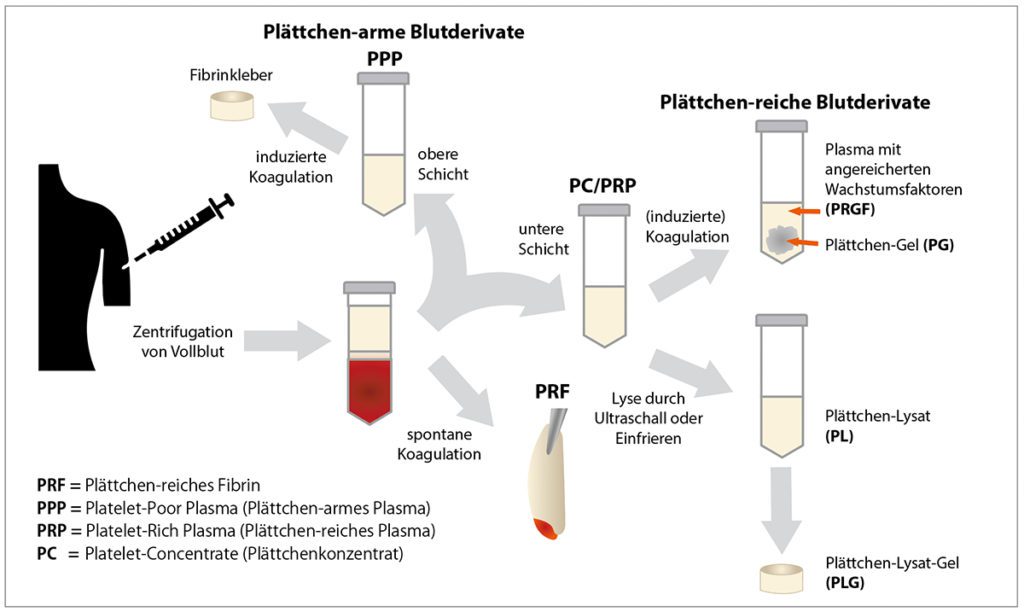
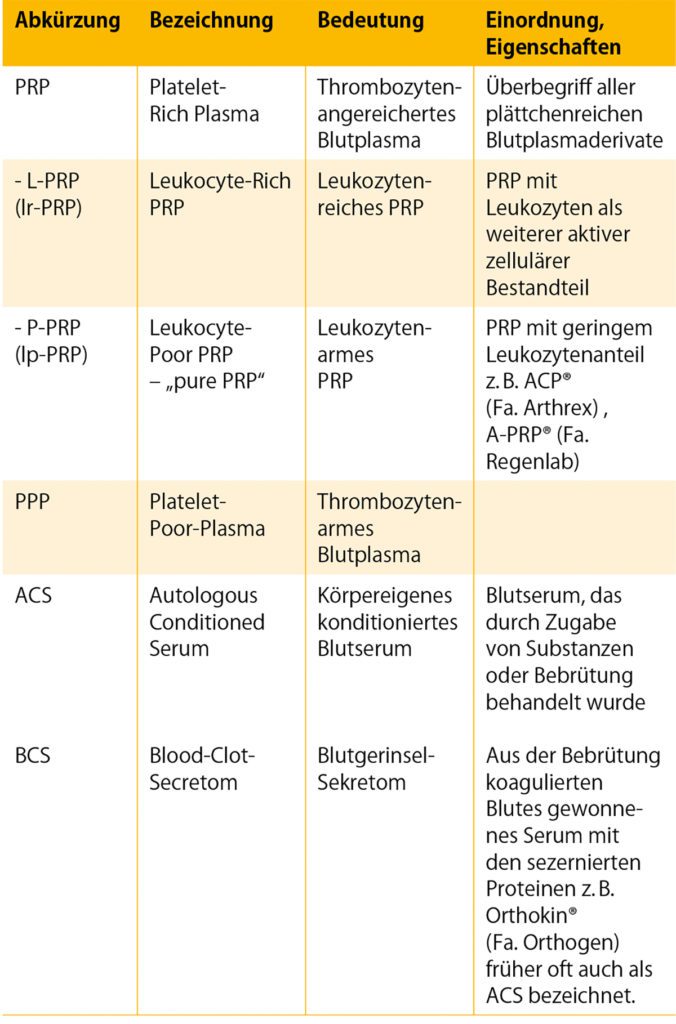
Beim sogenannten Platelet Rich Plasma handelt es sich durch ein aus dem Vollblut separierten Plasmaanteil, in dem die Thrombozyten zumeist durch Zentrifugation über deren Konzentration im Vollblut angereichert sind. Im Gegensatz z. B. zu den USA gibt es in Deutschland keine Vorgaben, welche Konzentration ein Verfahren erreichen muss, um als PRP-Produkt bezeichnet und angeboten werden zu können. In der Regel sollte aber eine Anreicherung um das 2 – 5- fache erreicht werden, um einen therapeutischen Nutzen zu erzielen. Bei der Zentrifugation kommt es zu einer Aufteilung der Blutbestandteile nach deren Größe und Gewicht. In der obersten Schicht kommt es dabei zu einer Anreicherung von Plasma (inkl. der darin gelösten Proteine), der Thrombozyten, aber auch von Zellfragmenten/-bestandteilen etc. Die schwereren und größeren roten Blutkörperchen setzen sich in einer breiten Schicht nach unten ab. In der Zwischenschicht dieser beiden Fraktionen bildet sich ein Bereich, der vermehrt weiße Blutkörperchen enthält, der sogenannte „Buffy-Coat“. Je nachdem, ob Anteile dieser Zwischensicht mit separiert oder entfernt werden, entstehen leukozytenarme PRPs (lp-PRP) oder leukozytenreiche PRPs (lr-PRP). Ebenso kann die oberste Sicht nach Separation nochmals aufgetrennt werden, womit man einen besonders plättchendichten Anteil oder plättchenarmes Serum (PPP) erhält. Ob die Anwesenheit von Leukozyten im PRP die gewünschte Wirkung verstärkt, wird seit längerem kontrovers diskutiert und ist alles andere als wissenschaftlich geklärt. So legen immer mehr Studien nahe, dass leukozytenreiches PRP gerade bei Insertionstendinosen wie z. B. der lateralen Epicondylopathie am Ellenbogen besonders effektiv sind, während wiederum andere Arbeiten zeigen, dass durch eine hohe Konzentration der Immunzellen eine katabole und entzündliche Stoffwechsellage begünstigt wird, die z.B. bei Wundheilungsprozessen einen negativen Einfluss haben könnte. Der Überblick wird noch weiter dadurch kompliziert, dass auch die Behandlung des Bluts vor der Zentrifugation Einfluss auf die Zusammensetzung des späteren Präparats hat. So kann zum einen eine Zentrifugation aus dem unbehandelten autologen Blut erfolgen, wie z. B. beim ACP® (Autologes Conditioniertes Plasma) der Fa. Arthrex oder eine Konditionierung durchgeführt werden, z. B. durch eine Bebrütungsphase oder die Zugabe bioaktiver Stoffe wie Citrat, EDTA oder bestimmter Zytokine. Hier spricht man von konditionierten Serumderivaten (ACS).


ACS (Autologous Conditioned Serum)
Systematisch zu trennen von den Platelet Rich Plasma Präparaten sind die reinen Plasmaprodukte wie z. B. das Orthokin® der Fa. Orthogen. Hier enthält das Infiltrat bei richtiger Herstellung zum Schluss keine Zellen mehr, weder Thrombozyten noch Immunzellen, sondern deren durch Bebrütung und Zentrifugation angereicherte Sekretionsproteine (zumeist Zytokine). Weshalb diese Präparate mittlerweile auch als Blood Clot Secretom (BCS) bezeichnet werden. Bei der späteren Injektion werden hier also keine lebenden Zellen oder Zellbestandteile in relevanter Menge an den Injektionsort mehr gebracht. Ob dies gewünscht ist oder nicht, hängt von der jeweiligen Indikation ab. Überlastetes oder verletztes Gewebe befindet sich zumeist in einem Stresszustand, der mit einer Veränderung des Gewebshomöostase, also des pH-Wertes, des Sauerstoffgehaltes, der Energiebereitstellung und der Präsenz von Immunzellen einhergeht. Allerdings ist der Effekt bei der Zugabe größerer Mengen lebender Zellen in dieses Milieu, die stoffwechselaktiv sind und daher Energie und Sauerstoff benötigen und selbst nach Apoptose wieder abtransportiert, phagozytiert und verstoffwechselt werden müssen, bislang kaum erforscht. Dieser Umstand könnte eine von vielen möglichen Erklärungen sein, warum PRP- Injektionen bei Sportverletzungen und vor allem bei Überlastungsfolgen derart heterogene Ergebnisse liefern. Der gewünschte positive Effekt der injizierten Plättchen und gegebenenfalls Immunzellen könnte stark davon abhängen, ob deren Art und Konzentration zum momentanen Gewebsmilieu am Injektionsort passt und einen vorteilhaften, neutralen oder eher nachteiligen Effekt auslöst. Da es hierfür bisher keine klinisch einsetzbaren Messmethoden gibt und auch die Konzentration der Zellbestandteile selbst beim gleichen Präparat innerhalb eines Patienten von mal zu mal stark schwanken kann, ist dies weitgehend vorhersehbar. Anderseits zeigt sich bei der Anwendung von zellreichen Plasmapräparaten gerade bei größeren Gewebsdefekten wie Sehnen- oder Bandrupturen, Frakturen etc. oft eine beschleunigte Ausbildung einer belastungsfähigen Narbe. Es ist vorstellbar, dass der Zell-Clot, der sich nach einer PRP-Injektion im Verletzungsareal ausbildet, eine Stimulation der bindegewebigen Ausheilung über einen sehr viel längeren Zeitraum bewirken kann und dass die damit verbundene Auffüllung des Gewebedefekts mit Fibrin, Proteinen und Zellen eine Matrix für den Umbau in Narbengwebe darstellen könnte.
Fazit
Die Vor- und Nachteile der verschiedenen Präparate und damit deren Indikationen oder relativen Kontraindikationen hängen also stark von der jeweiligen Situation des Patienten, Art, Umfang und Lokalisation der Verletzung ab, ebenso aber auch von den Erfahrungen und dem Wissen des jeweiligen Anwenders. Generell kann man aus der praktische Erfahrung festhalten, dass der Einsatz nur einer Zubereitungsklasse für alle muskuloskelettalen Indikationen sicher nicht optimal ist. Es ist die Aufgabe von Wissenschaftlern, aber auch von Praktikern, die Erfahrungen über die Einsätze, Ergebnisse und Verläufe der Anwendung der einzelnen Präparate zu sammeln und uns kritisch, offen und seriös darüber auszutauschen. Nur so können wir es schaffen, aus dem steigenden Angebot verschiedener Präparate die jeweils für unseren Patienten richtigen auszuwählen und so dafür zu sorgen, dass die Zuverlässigkeit und Akzeptanz für diese Verfahren bei Sportlern, Kollegen und Versicherungsträgern weiter steigt.


Literatur beim Autor
Autoren
ist Facharzt für Orthopädie und Unfallchirurgie. Er ist seit 2018 festangestellter Mannschaftsarzt von Borussia Mönchengladbach, zusätzlich arbeitet er im Orthopädiezentrum Theresie in München. Zuvor war Dr. Doyscher in verschiedenen Abteilungen der Charité Berlin tätig. Außerdem war er Mannschaftarzt des 1. FC Union Berlin sowie Verbandsarzt des DLV und BSD. Dr. Doyscher ist wiss. Beirat der sportärztezeitung.
ist Facharzt für Orthopädie und Unfallchirurgie und arbeitet in der ATOS-Klinik München. Seit 2002 ist er Mannschaftsarzt der Deutschen Ski-Nationalmannschaft alpin und Verbandsarzt des Deutschen Skiverbandes (DSV), seit 2015 leitender Mannschaftsarzt des DSV. Er ist Kniespezialist mit dem Schwerpunkt auf regenerative und rekonstruktive Verfahren sowie Muskel-Sehnenverletzungen an der unteren Extremität.