Je nach Sportart variiert die Inzidenz von Leistenproblemen. So fanden Emery et al. bei Eishockeyspielern der nordamerikanischen Hockey-Liga (NHL) eine Leistenverletzung in zwischen 13 und 20 % der Fälle. Unter männlichen Fußballspielern liegt die Inzidenz für chronischen Leistenschmerz bei bis zu 18 %.
Differenzialdiagnostik von Leistenschmerzen
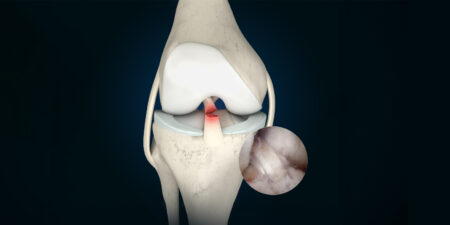
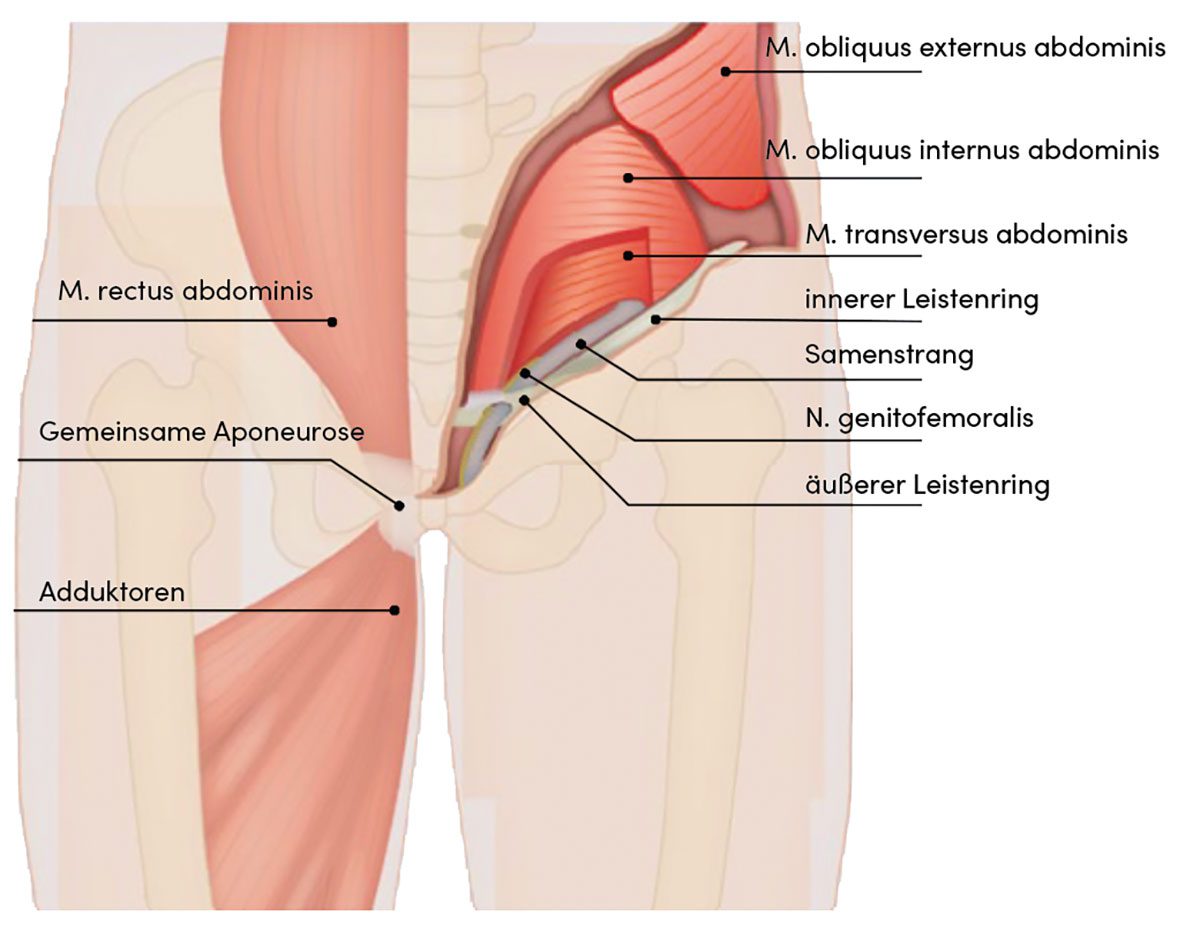
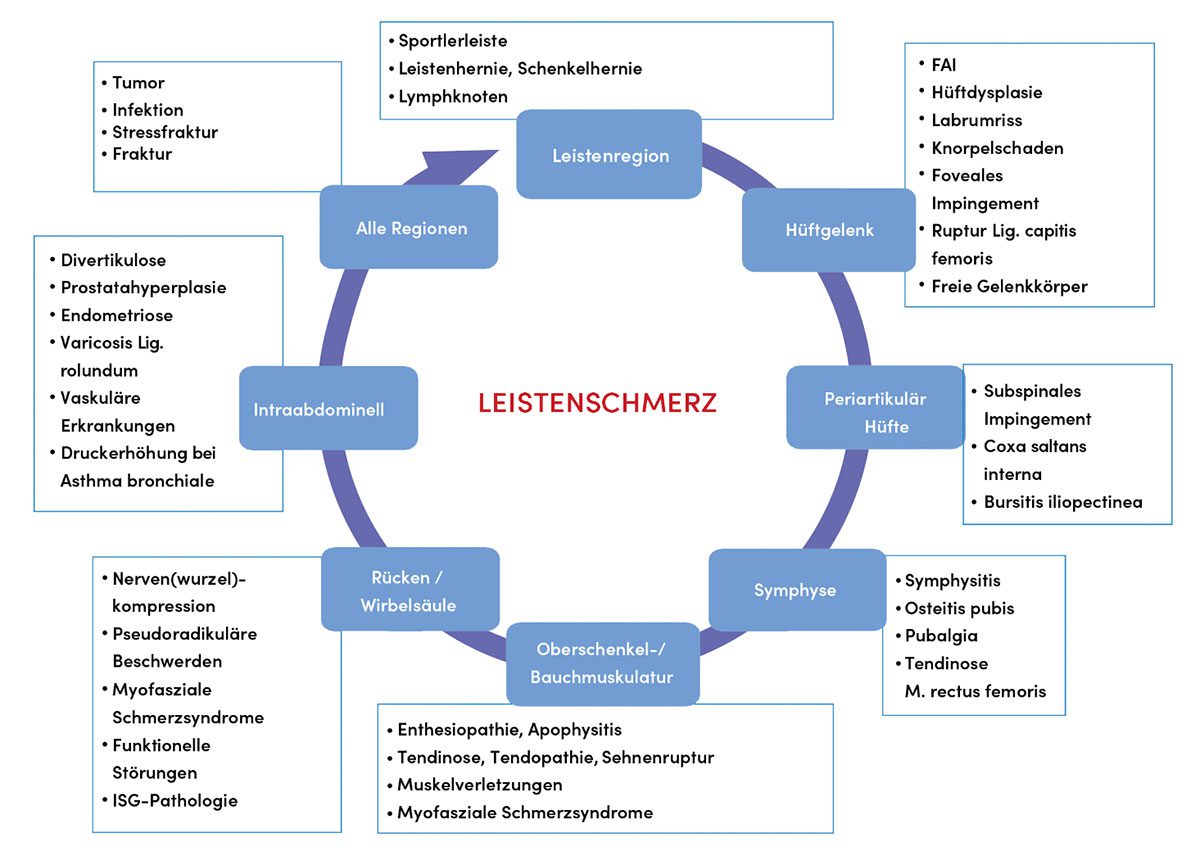
Betroffen von Leistenschmerzen sind vor allen Sportler, deren Bewegungsablauf durch eher einseitige körperliche Belastungen mit schnellen, wechselnden Bewegungen gekennzeichnet ist. Gerade bei Fußballspielern, die im Laufschritt tretende und drehende Bewegungen ausführen mit schnellen abrupten Richtungswechseln, kombiniert mit kraftvollem Schießen des Balles, ist der akut einsetzende Leistenschmerz häufig zu beobachten. Eine klare Differenzierung der zugrundeliegenden Pathologie ist entscheidend, um unnötige Operationen zu vermeiden, dauerhaften Schäden vorzubeugen und den Patienten einer zielgerichteten Therapie zuzuführen. Der Begriff „Leiste“ geht auf das germanische Wort „leisto“ zurück, das „Rand“ bedeutet. Dieser „Rand“ beschreibt den Übergang des Rumpfs zum Oberschenkel. Sie ist auch ein Teil der vorderen Bauchwand, einer Funktionsgemeinschaft von Muskulatur und Aponeurosen, die in ihrem distalen Anteil den Leistenkanal bilden. Die dadurch entstehenden muskulofaszialen Verspannungssysteme ermöglichen erst die Lastenverteilung und -weiterleitung auf das knöcherne Skelett. Gerade die gemeinsame Aponeurose von M. rectus abdominis und M. adductor longus wird bei sportlicher Belastung stark beansprucht (Abb. 1). Aber auch benachbarte anatomische Strukturen wie das Hüftgelenk, das Schambein sowie die Rücken- und Oberschenkelmuskulatur können Auslöser von Beschwerden sein, die sich auf die Leiste projizieren (Abb. 2). Die in Abb. 2 zusammengefassten häufigsten Differenzialdiagnosen von Leistenschmerzen bei Sportlern zeigen, dass Leistenschmerzen weit mehr Ursachen haben können als nur eine „weiche Leiste“.
Diagnostik
Primär gilt es, zunächst zwischen intraartikulären Hüftgelenkspathologien und extraartikulären Ursachen zu unterscheiden. Im Weiteren erfolgen eine Differenzierung lokaler Veränderungen des Stütz- und Bewegungsapparates und des Bindegewebes von fortgeleiteten Schmerzen sowie die Unterscheidung von funktionellen Störungen und strukturellen Veränderungen. Nicht selten liegen dabei mehrere pathologische Veränderungen gleichzeitig vor. Bei der Vielzahl an möglichen Ursachen für Leistenschmerzen kommt der sorgfältigen Anamnese und klinischen Untersuchung eine zentrale Bedeutung zu. Danach sollte eine entsprechend zielgerichtete apparative Diagnostik erfolgen.
Schmerzanamnese
Bei der Schmerzanamnese geht es darum, den Schmerzcharakter so genau wie möglich zu erfragen. Durch eine sorgfältige Anamnese lassen sich mögliche Schmerzursachen häufig bereits eingrenzen (Tabelle 1).

Klinische Untersuchung
Die körperliche Untersuchung sollte am entkleideten Patienten im Stehen beginnen. Zum Ausschluss der häufigsten Differenzialdiagnosen der „Sportlerleiste“ sollte bei der klinischen Untersuchung vor allem auf Dysfunktionen des Iliopsoaskomplexes, der Adduktoren und des M. rectus abdominis geachtet werden. Bei Leistenschmerzen sollte stets das Hüftgelenk auf klinische Auffälligkeiten untersucht werden. Gerade mechanische Ursachen von Labrum- und Knorpelschäden wie das femoroacetabuläre Impingement (FAI) sind bei Profisportlern häufig. Die spezifische Untersuchung der Leiste selbst beginnt mit einer Palpation, zunächst mit flachen Fingern über der Leiste in Ruhe, dann gefolgt von einer intermittierenden intraabdominellen Druckerhöhung durch den Patienten, z. B. durch Husten oder Pressen. Beim männlichen Patienten lässt sich durch Mitfassen von Skrotalhaut die Fingerspitze in Richtung äußerer Leistenring vorlegen. Hier lässt sich eine mögliche Bruchpforte und/oder Protrusion der Leistenkanalhinterwand tasten, was häufig als unangenehm und/oder schmerzhaft empfunden wird. Auch hier erfolgt die Untersuchung zunächst in Ruhe und dann unter intraabdomineller Druckprovokation (Valsalva-Manöver).
Ultraschall
Aufgrund der statischen als auch dynamischen Untersuchungsbedingungen kommt dem Ultraschall in der Abklärung der Sportlerleiste eine besondere Bedeutung zu. Besonders wichtig ist auch während der Untersuchung die intermittierende Erhöhung des intraabdominellen Druckes durch wiederholtes Pressen (Valsalva-Manöver). Häufig gelingt erst durch dieses Manöver, eine Vorwölbung der Leistenkanalhinterwand oder einen Fasziendefekt darzustellen. Dabei reicht der alleinige sonographische Befund einer Protrusion der Leistenkanalhinterwand für die Diagnosestellung nicht aus. Vielmehr muss dies mit den typischen klinischen Symptomen einhergehen. So konnten Orchard et al. bei australischen Footballspielern eine sonographische Vorwölbung in 20 % nachweisen, ohne dass diese Spieler Beschwerden hatten.
Konventionelles Röntgen
Die Standarddiagnostik zur Abklärung von Hüftgelenkserkrankungen und knöchernen Pathologien umfasst eine Beckenübersicht sowie eine Aufnahme des betroffenen Hüftgelenkes womit die häufigsten Knochen- und Gelenkpathologien erfasst werden können.
Magnetresonanztomographie
Die MRT ist heute ein häufig eingesetztes Verfahren zur Abklärung von Leistenschmerzen. Zur Beurteilung von knöchernen Veränderungen, Symphysitis, Weichteilschwellungen, Raumforderungen und Ansatztendinosen ist eine MRT des Beckens nach durchgeführter nativer Röntgendiagnostik das Verfahren der Wahl. Für die Sportlerleiste gibt es hingegen in der MRT keine eindeutigen und reproduzierbaren Untersuchungsbefunde. Häufig findet sich ein Knochenmarködem im Bereich des Schambeines, das aber nicht pathognomonisch sein muss.
Infiltration bei differenzialdiagnostischer Unsicherheit
Zur Differenzierung Pubalgie und Leistenschmerz können probatorische Infiltrationen hilfreich sein. Eine Osteitis pubis lässt sich nicht durch einen Ileoinguinalen Block beeinflussen. Die Schmerzfreiheit nach Ileoinguinalem Block kann wegweisend zur Indikation für ein operatives Vorgehen bei der Sportlerleiste sein.
Sportlerleiste – ein pathophysiologische Ansatz
Die Nomenklatur ist erstaunlich vielseitig: Man spricht von der „Sportlerleiste“, der „Sportlerhernie“, der „weichen Leiste“, der „Hernia incipiens“, der „Symphysitis“, der „Pubalgie“, dem „pubic inguinal pain syndrome“ (PIPS), der „pubic bone stress injury“, dem „Dysbalance-Syndrom“, der „Gilmore‘s groin“ oder der „inguinal disruption injury“. Kaum ein Beschwerdekomplex wird zwischen Sportmedizinern, Orthopäden und Chirurgen so kontrovers diskutiert wie dieser. Viele Autoren haben sich an einer pathophysiologischen Erklärung und entsprechenden Definition versucht, von denen sich aber keine durchsetzen konnte. Einigkeit besteht heute nur darüber, dass es sich nicht um eine klassische Hernie handelt. Der Begriff „Gilmore‘s groin“ wurde 1980 von O.J. Gilmore geprägt. Er beschreibt eine Schwächung oder Ausdünnung des M. obliquus externus und seiner Faszie bzw. Dilatation des äußeren Leistenrings in Verbindung mit einer Separation der „conjoint tendon“ vom Leistenband und Schlaffheit der Transversalisfaszie. Das „imbalance syndrome“ oder auch „dysbalance syndrome“ erklärt die Beschwerdesymptomatik durch den Muskelzug des M. rectus abdominis auf der einen Seite und dem M. adductus longus auf der Gegenseite der Symphyse. Die physiologische Biomechanik wird dadurch gestört und es kommt zu Einrissen an den Sehnenansätzen. Dies kann wiederum einen Leistenschmerz auslösen. Meyers spricht von einem „pubic joint“ und schreibt dem Leistenband und Schambein eine gelenkartige Funktion zu. Die „Osteitis pubis“ entsteht durch repetitiven Stress des muskulotendinösen Komplexes am Schambeinansatz. Auch eine vermehrte Spannung durch Muskelzug am Os pubis, wie bei der Sportlerleiste durch Retraktion des M. rectus abdominis, kann dafür ursächlich sein.
Die bisherigen Definitionsversuche bleiben aber unbefriedigend und sehen den Beschwerdekomplex der Sportlerleiste eher als eine Ausschlussdiagnose. Im Gegensatz dazu sehen wir in der Sportlerleiste keine Ausschlussdiagnose, sondern eine klare abgrenzbare Pathologie, die durch typische Beschwerden, reproduzierbare klinische und sonographische Untersuchungsergebnisse untermauert und den intraoperativen Befund belegt ist. Eigene Definition: Bei der Sportlerleiste liegt eine umschriebene Schwäche im medialen Anteil der Leistenkanalhinterwand vor. Hierdurch kommt es zu einer lokalisierten Vorwölbung der Transversalisfaszie nach ventral in den Leistenkanal hinein. Dies führt bei Anspannung der Bauchdeckenmuskulatur und bei abrupten Bewegungen zu einem für die Sportlerleiste typischen Schmerz, welcher durch Kompression des R. genitalis des N. genitofemoralis hervorgerufen wird. Zusätzlich führt diese Schwäche der Leistenkanalhinterwand zu einer Erweiterung des Leistenkanals mit Retraktion des lateralen Anteils des M. rectus abdominis an seinem Ansatz am Os pubis (Abb. 3). Dies erklärt die lokalisierten Schmerzen und konsekutiv die Entwicklung eines Knochenmarködems im Bereich des Os pubis (Pubalgia athletica, Osteitis pubis). Dieser pathophysiologische Ansatz deckt sich mit den Ergebnissen von Swan und Wolcott, die in einer Übersichtsarbeit vor allem eine Schwäche in der Hinterwand des Leistenkanals als Ursache für die chronischen, aktivitätsbezogenen Leistenschmerzen beschreiben. Unterstützend für die Definition der Sportlerleiste als Schwäche der Leistenkanalhinterwand mit konsekutiver Nervenkompression sind auch die eigenen Ergebnisse der histologischen Aufarbeitung der resezierten Nervenanteile des R. genitalis. Hierbei konnte immer eine perineurale Fibrose nachgewiesen werden.

R. genitalis des N. genitofemoralis (gelb). b Verlagerung der am Schambein ansetzenden Rektusmuskulatur nach kraniomedial (grauer Pfeil) mit Zunahme der Spannung am Os pubis (Pubalgia athletica). a, b
(Mit freundl. Genehmigung © U. Muschaweck 2014. All rights reserved)
Therapie der Sportlerleiste
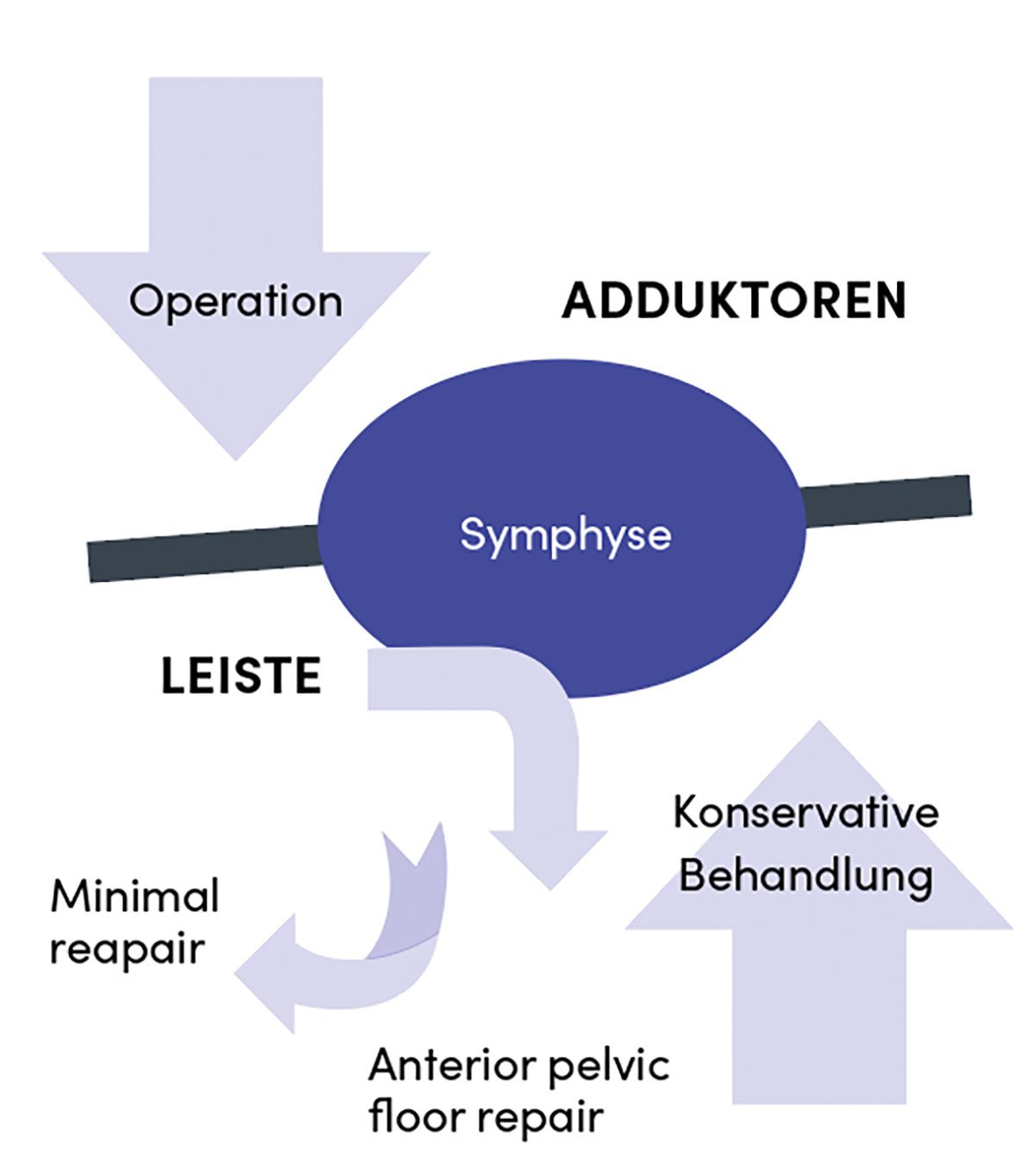
Bei der Versorgung von Sportlerleisten wird das ideale Therapiekonzept weiterhin kontrovers diskutiert. Es fehlen prospektiv randomisierte Studien, welche die verschiedenen therapeutischen Ansätze und Verfahren vergleichen. Der Evidenz liegen nur Kasuistiken und Kohortenstudien (Level III–IV) sowie Expertenmeinungen (Level V) zugrunde. Ein Positionspapier der Britischen Hernia Society besteht ebenfalls nur aus der Sammlung von Expertenmeinungen. Die Therapie richtet sich vor allem nach der „vermuteten“ zugrundeliegenden Ursache. Sie reicht von Schonung und anschließenden konservativen Trainingsprogrammen bis hin zu teils aufwendigen Operationen. Grundsätzlich gilt, je mehr die Beschwerden in Richtung Symphyse/Adduktoren ausstrahlen, desto eher sollte zunächst ein konservativer Ansatz gewählt werden und vice versa; je mehr nach inguino-skrotal, desto eher operativ (Abb. 4).
Konservative Therapie
Vor allem traumatische Ursachen des Leistenschmerzes, Zerrungen, Risse, Entzündungen und Reizungen sind der konservativen Therapie zugänglich. Häufig können durch antiinflammatorische Medikation und/oder lokale Injektion von Kortikosteroiden, Traumeel und Dextrose die Beschwerden gebessert werden. Ergebnisse zur Eigenblutbehandlung/plättchenreichem Plasma (PRP) liegen noch nicht in größerer Fallzahl vor. Intensive physiotherapeutische Programme mit Stretching und Friktionsbehandlungen sowie Massagen haben einen wichtigen Stellenwert im Rahmen der sportlichen Rehabilitation. Zusätzlich werden Koordinations- und Stabilisationsübungen zum Ausgleich muskulärer Dysbalancen sowie osteopathische Maßnahmen durchgeführt.
Operative Therapie
Prinzipiell werden drei unterschiedliche operative Verfahren diskutiert, welche die verschiedenen pathophysiologischen Ansätze widerspiegeln, die aber auch häufig kombiniert werden: Geht man von einer Nervenkompression aus, so sollte eine lokale Neurolyse oder Neurektomie erfolgen. Für die „Imbalance“ der beteiligten Muskulatur werden neben Refixationen des lateralen Rektusmuskelrandes auch sog. Releasing-Verfahren vorgeschlagen, partielle Tenotomien von M. rectus und/oder Adduktorenmuskulatur bis hin zur laparoskopischen Durchtrennung des Lig. inguinale. Außerdem wird die Stabilisierung der umschriebenen Schwäche/Vorwölbung der Leistenkanalhinterwand mit oder ohne Netzverstärkung empfohlen. Im Jahr 2002 wurde auf dem 111. Internationalen Fußballkongress in Madrid erstmals ein neues offenes Nahtverfahren zur Versorgung von Sportlerleisten vorgestellt, die Minimal-Repair-Technik nach Muschaweck, diese wurde durch die Autorin auch 2002 in Hernia erstmals publiziert. Hierbei wird selektiv der Hinterwanddefekt unter Schonung der intakten Anteile mittels einer Fasziendopplung repariert. Durch Einbeziehung des lateralen Rektusrandes in die Nahtreihe wird dieser lateralisiert und die bei einer Sportlerleiste erhöhte Spannung am Schambeinansatz reduziert. Wichtig ist hierbei die Möglichkeit, eine Schädigung des komprimierten R. genitalis zu erkennen und ggf. eine Neurolyse oder Neurektomie zeitgleich durchzuführen. Diese Beurteilung ist bei einem laparoskopischen Vorgehen nicht möglich und birgt das Risiko der Schmerzpersistenz durch Belassung des geschädigten Nervens. In einer prospektiven Kohortenstudie mit 129 Patienten, davon 67 % professionelle Sportler, konnte die Effektivität der Minimal-Repair-Technik nachgewiesen werden. Nach 14 Tagen waren 80 % der Sportler beschwerdefrei und konnten an ihre alte Form anknüpfen.
Nachbehandlung
Die Rekonvaleszenz nach einem erfolgten operativen Eingriff umfasst in der Regel einen Zeitraum von mindestens 2 – 6 Wochen. Die Nachbehandlung sollte in enger Zusammenarbeit mit einem speziell ausgebildeten Physiotherapeuten erfolgen. Gerade nach offenen Nahtverfahren, wie dem Minimal-Repair, ist eine schnelle Rückkehr zur normalen Aktivität und Wiederaufnahme des sportlichen Trainings möglich. Bei komplexeren operativen Eingriffen wie dem „Anterior pelvic floor repair“ nach Meyers ist eine Rückkehr zum vollen Training oft erst nach 8 – 12 Wochen realistisch.
Autoren
ist Facharzt für Chirurgie und Viszeralchirurgie in eigener Praxis für Viszeral- und Hernienchirurgie in Cottbus. Er ist seit 2003 Mannschaftsarzt des FC Energie Cottbus und außerdem kooperierender Arzt des Olympiastützpunktes Cottbus sowie des DEL2 Teams der Lausitzer Füchse.
ist Fachärztin für Chirurgie und gründete 1993 mit dem Hernienzentrum Muschaweck in München das erste ambulante OP-Zentrum für Hernienchirurgie in Deutschland. Sie ist als Hernienspezialistin in Starnberg, München und London tätig und zusätzlich Mitglied der Deutschen, Europäischen und Amerikanischen Herniengesellschaft.