Die Arthroseprävalenz steigt und erfordert die Weiterentwicklung und Optimierung konservativer, multimodaler Therapiekonzepte. In diesem Kontext hat sich der Einsatz von Hylauronsäureprodukten im sportmedizinisch-orthopädischen Praxisalltag etabliert. Obwohl der Effekt von intraartikulär verabreichter Hyaluronsäure (IA-HA) weiterhin kontrovers diskutiert wird, wächst der Markt für Viskosupplemente (VS) stetig (2021: $ 4,4 Mrd.; prognostiziert bis 2031: $ 10,9 Mrd.) [1]. Neue Wirkstoffkombinationen und Produktinnovationen treiben die Marktentwicklung voran und führen zu einer Vielzahl wissenschaftlicher Publikationen [2].
Um die Effizienz des Einsatzes von IA-HA zu erhöhen, müssen die Unterschiede von HA-Produkten verstanden und beachtet werden. Hyaluronsäureprodukte in der Sportmedizin: Wissenschaftlicher Diskurs vs. Praxiserfahrungen – der Versuch einer Einordnung
Arthroseprävalenz
Im Jahr 2020 waren weltweit 595 Millionen Menschen – 7,6 % der Gesamtbevölkerung – von Arthrose betroffen. Eine im Lancet (2023) veröffentliche Prognose schätzt, dass bis 2050 rund eine Billion Menschen weltweit von Arthrose betroffen sein könnten, sofern sich der aktuelle Trend fortsetzt [3]. In Deutschland lag die Arthroseprävalenz der Erwachsenen 2019 bei 17,1 % [4]. Mit zunehmendem Alter steigt die Häufigkeit deutlich: Ab 65 Jahren waren ca. 48 % der Frauen und 31 % der Männer betroffen. Der demografische Wandel lässt einen weiteren Anstieg der Arthroseprävalenz erwarten [5]. Das Knie ist das am häufigsten betroffene Gelenk. Die altersstandardisierte Prävalenz der Kniearthrose (KOA) lag 2020 weltweit bei ca. 4.307 Fällen pro 100.000 Menschen. Symptomatische KOA führt häufig zu starken Schmerzen, einer limitierten Mobilität und deutlichen Einschränkungen der Lebensqualität durch reduzierte Selbstständigkeit bei Alltagsaktivitäten [6, 7]. Aufgrund der hohen sozio-ökonomischen Belastung durch muskuloskelettale Erkrankungen rief die World Health Organization (WHO) die Bone and Joint Decade ins Leben, um die Forschung und Versorgung zu verbessern und den wachsenden Herausforderungen im Gesundheitssystems zu begegnen [5].
Aktuelle Empfehlungen
Der Effekt von IA-HA wird in der wissenschaftlichen Fachliteratur kontrovers diskutiert und erfordert eine differenzierte Betrachtung des Evidenzkorpus. Die Empfehlungen internationaler klinischer Leitlinien weichen teils erheblich voneinander ab und geben unterschiedliche Empfehlungen zum Einsatz von IA-HA bei KOA [8]. Die Veröffentlichung der neuen S3-Leitlinie „Prävention und Therapie der Gonarthrose“ der Deutschen Gesellschaft für Orthopädie und Unfallchirurgie e.V. (DGOU) wird in Kürze erwartet. Bis dahin stützen sich die Empfehlungen weiterhin auf die aktualisierte S2k-Leitlinie „Gonarthrose“, die für IA-HA die offene Empfehlung „kann erwogen werden“ ausspricht:
„Bei der Konsensabstimmung hat, vor dem Hintergrund der vorliegenden Evidenz, die offene Empfehlung („kann erwogen werden“) von intraartikulärer HA-Injektion bei Patient*innen, bei denen der Einsatz von NSAR kontraindiziert ist oder bei denen NSAR nicht ausreichend wirksam sind, eine mehrheitliche Zustimmung erreicht (63 %). Die offene Empfehlung („kann erwogen werden“) über kombinierte, simultane Injektion von HA mit Corticosteroiden bei Patient*innen, bei denen ein entzündlicher Schub im Vordergrund steht, erzielte ebenso eine mehrheitliche Zustimmung (63 %).“ [9]
Laut einer kürzlich veröffentlichen Übersichtsarbeit zu den „current clinical practice guidelines“ ist IA-HA in globalen Leitlinien Bestandteil des Therapiemanagements bei KOA [10]. Basierend auf den Ergebnissen eines „Delphi consensus processes“ veröffentliche ein Expertenpanel der „EUROVISCO group“ 2024 consensus guidelines für IA-HA bei KOA: Die 34 resultierenden Statements mit zum Teil starken Empfehlungen für IA-HA Injektionen [11] können klinisch Tätigen als Grundlage für die Erarbeitung individueller Behandlungsalgorithmen dienen. Bei der Auswahl der VS sollte zudem die Kosten-Nutzen-Effektivität von Hyaluronsäureprodukten im Hinblick auf bspw. deren biochemische Zusammensetzung und Wirkstoffkombinationen sowie unterschiedliche Patientenkollektive beachtet werden [2]. Zum Outcome Schmerz zeigte eine Netzwerkmeta-Analyse nach IA-HA Applikation eine MCID und eine Effektgröße 0,34 – 0,63 und damit bessere Ergebnisse als bei der mit Corticosteroiden und Paracetamol therapierten Kontrollgruppe [12]. Andere systematische Evidenz zeigte hingegen nur eine geringe Schmerzreduktion nach IA-HA und damit keine klinische Signifikanz [13]. Kurzzeitige Schmerzlinderung nach IA-HA konnte in einer 2024 publizierten systematische Übersichtsarbeit zu RCTs gezeigt werden [14]. Eine 2024 zu diesem Thema veröffentlichte Literaturanalyse verdeutlicht unterschiedliche Angaben zu Effektstärken und beschreibt Hinweise auf vorliegenden Publikationsbias [15]. Folglich sollte die Ableitung der klinischen Relevanz unter Berücksichtigung benannter Aspekte erfolgen.
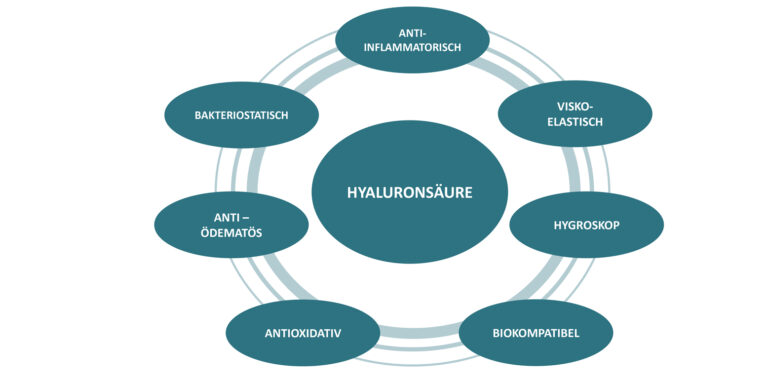
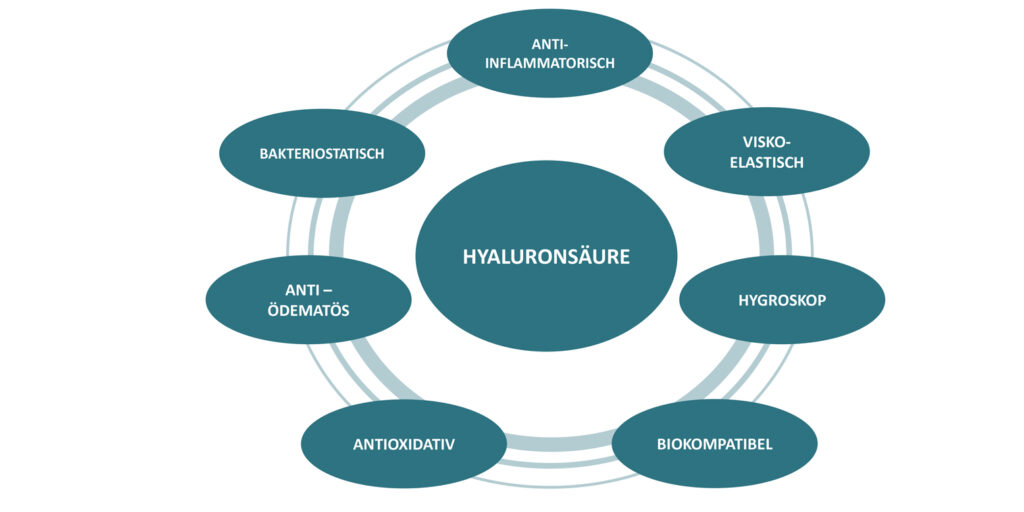
Eigenschaften und Wirkweise von Hyaluronsäure (Abb. 1)
Erfahrungen aus dem sportmedizinisch-orthopädischen Praxisalltag: Gute Verträglichkeit mit geringer Nebenwirkungsrate (Obligat: Intraartikuläre Injektionen unter aseptischen Bedingungen) ► Ähnlichkeit zur physiologischen Gelenksituation / Homöostase – Induktion der körpereigenen HA-Synthese; minimalinvasive Behandlungsmöglichkeit; gute Verträglichkeit in Kombination mit anderen Orthobiologischen Präparaten; positive Effekte auf PROMs.
Zu beachtende Punkte: Kontraindikationen gegenüber Inhaltsstoffen; Kostenerstattung; Verweildauer im Gelenk – Langzeitwirkung; Qualität der IA-Injektion; Variabilität der Ergebnisse in Abhängigkeit des Arthrosegrades und Patientenkollektivs.
Produktübersicht und Erfahrungen aus dem sportmedizinisch-orthopädischen Praxisalltag
Die folgenden Tabellen bieten einen exemplarischen Überblick über HA-Produkte für IA-Anwendung. Zur Übersichtlichkeit sind die Tabellen nach Struktur und Wirkstoffzusammensetzung der HA-Produkte aufgeteilt, die Inhalte beziehen sich auf die Herstellerangaben.
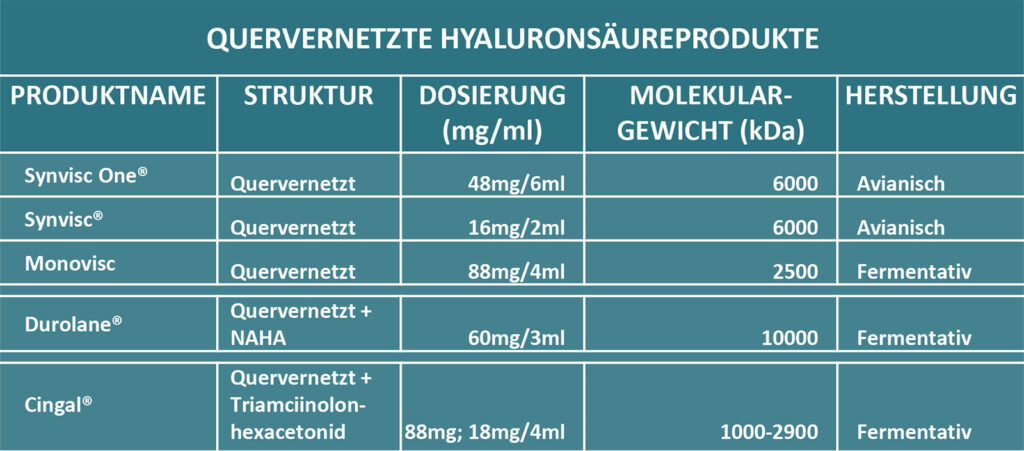
Quervernetzte Hyaluronasäureprodukte (Tab. 1)
Erfahrungen aus dem sportmedizinischorthopädischen Praxisalltag: Quervernetzte Hylauronsäuren zeigten positive Ergebnisse bei älteren Patienten mit fortgeschrittener Arthrose.
Lineare Hyaluronsäureprodukte (Tab. 2)
Erfahrungen aus dem sportmedizinisch-orthopädischen Praxisalltag: Die Kombination von linearen Hyaluronsäureprodukten mit Mannitol oder Sorbitol scheint durch die Wirkstoffkombination die Verweildauer der Hyaluronsäre im Gelenk zu erhöhen. Nach IA-Injektion von linerarer-HA mit Sorbitol bei jungen Sportlern zeigten sich langfristig positive Ergebnisse auf PROMs.
Ein HA-Produkt mit Sobitol wird im Folgenden ausführlicher betrachtet. Zu diesem Produkt liegen neue Studienergebnisse bspw. zum Effekt auf das Outcome Schmerz und auf die Biomechanik von KOA Patienten vor.
Produktvarianten: Synolis VA 40 / 80; 80 / 160
- Viskoelastische, sterile, apyrogene, isotonische, gepufferte 2 %ige Natriumhyluronatlösung
- Natriumhyluronat: Bakterielle Fermentation
- Molekulargewicht: 2000 kDa
- Neutraler pH-Wert (6,8 – 7,4 %) (Ähnlichkeit zur Synovialflüssigkeit)
Hohe 2 % Konzentration & hohes Molekulargewicht des Natriumhyluronats in Kombination mit Polyol (Sorbitol) (Einschränkung der Zersetzung) -> verleiht viskoelastischer Lösung die Fähigkeit, Gelenkschmierungs- und Schockabsorptionseigenschaften wiederherzustellen [17, 18].
In einer Beobachtungsstudie zeigten sich durch die Kombination von HA mit Sorbitol zwei mögliche Eigenschaften: 1. Sorbitol fungiert als „Fänger“ freier Radikale, 2. Sorbitol schützt HA vor freien Radikalen und verlängert dadurch die Wirkstoffverfügbarkeit der HA [19].
In einer einarmigen Interventionsstudie erhielten (n = 33) Probanden mit KOA eine IA-HA und Sorbitol Injektion. Die Evaluation der primären Outcomes Schmerz und Funktion erfolgte nach 1-, 3- und 6 Monaten. Signifikante Ergebnisse bzgl. Schmerzreduktion werden beschrieben [20]. Die positiven Ergebnisse sollten unter Beachtung vorliegender Studienlimitationen (bspw. begrenzte Stichprobe, keine Kontrollgruppe) eingeordnet werden. Eine 2024 publizierte Studie zeigte kurz- und langfristige positive Effekte auf die Biomechanik (kinematische Veränderungen) von Patienten mit fortgeschrittener KOA nach VS [21].
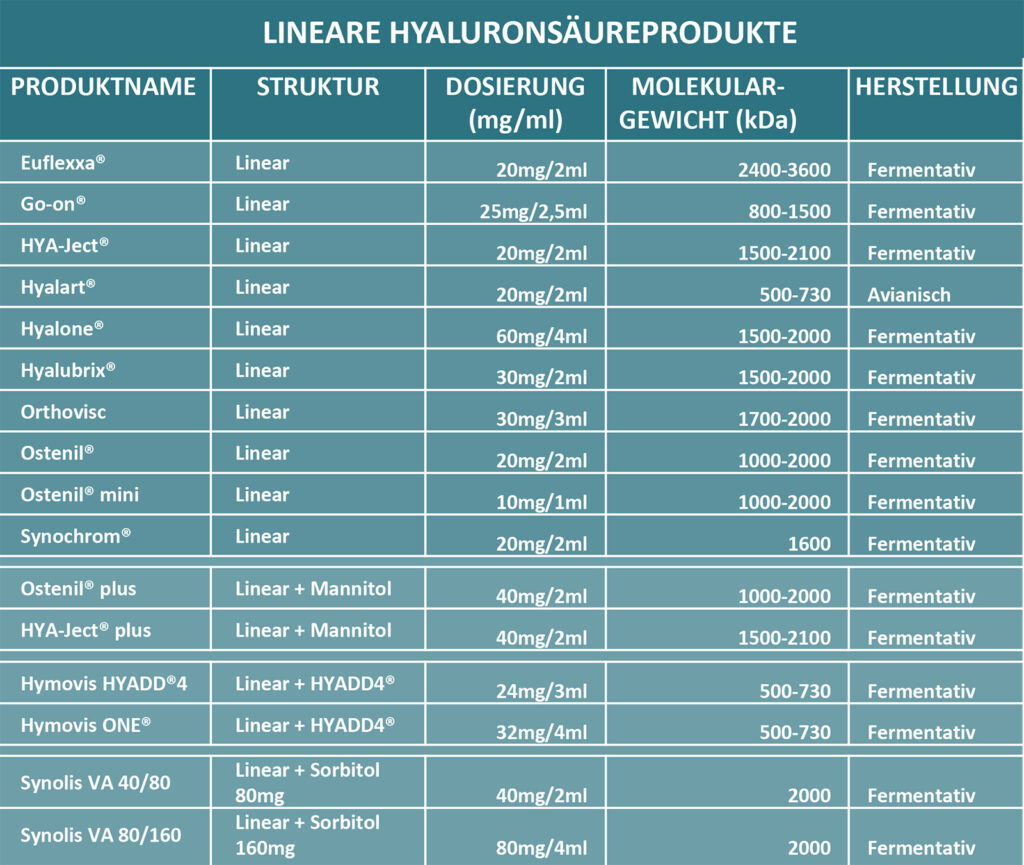
Tab. 2 Lineare Hyaluronsäureprodukte (eigene Abbildung nach Herstellerangaben)
Hybridprodukte (Tab. 3)
Erfahrungen aus dem sportmedizinisch-orthopädischen Praxisalltag: Zu den Hybridprodukten liegen uns aktuell nur vereinzelt Erfahrungen aus dem sportmedizinisch-orthopädischen Praxisalltag vor. Ein ausführlicher Erfahrungsbericht wird im nächsten Update aufgeführt.

Fazit
IA-HA kann als ein „wichtiger“ Bestandteil eines multimodalen Arthrosemanagements angesehen werden [11]. Die Produktauswahl sollte unter Beachtung der Produktunterschiede erfolgen. Es bedarf einer kontinuierlichen Weiterentwicklung und Optimierung von Behandlungsalgorithmen mit orthobiologischen Therapieoptionen (bspw. PRP, Kollagen, ACS). Weitere Ziele:
- Verbesserung der klinischen Outcomes
- Verbesserung der klinischen Wirksamkeit durch innovative Wirkstoffkombinationen – Produktentwicklungen
- Optimierung des indikationsspezifischen Einsatzes von HA-Präparaten (Unterschiede Wirkstoffkombinationen etc.) im Behandlungsalgorithmus weiterer orthobiologischer Therapieverfahren
- Aufarbeitung des Forschungsbedarfs unter Beachtung aktueller Studienlimitationen (Vermeidung von
„research waste“)
Literatur
- Allied Market Research. Viscosupplementation market research, 2031. Verfügbar unter: https://www.alliedmarketresearch.com/viscosupplementation-market.
- Ferkel E, Manjoo A, Martins D, Bhandari M, Sethi P, Nicholls M. Intra-articular Hyaluronic Acid Treatments for Knee Osteoarthritis: A Systematic Review of Product Properties. Cartilage. Dezember 2023;14(4):424–32.
- Steinmetz JD, Culbreth GT, Haile LM, Rafferty Q, Lo J, Fukutaki KG, u. a. Global, regional, and national burden of osteoarthritis, 1990–2020 and projections to 2050: a systematic analysis for the Global Burden of Disease Study 2021. Lancet Rheumatol. 1. September 2023;5(9):e508–22.
- Robert-Koch-Institut. Arthrose: Prävalenz (ab 18 Jahre) Gesundheitsberichterstattung des Bundes. [Internet]. 2024. Verfügbar unter: https://gbe.rki.de/
- Fuchs J, Kuhnert R, Scheidt-Nave C. 12-Monats-Prävalenz von Arthrose in Deutschland. 2. Aufl. 2017; Verfügbar unter: DOI 10.17886/RKI-GBE-2017-054
- Migliorini F, Tingart M, Niewiera M, Rath B, Eschweiler J. Unicompartmental versus total knee arthroplasty for knee osteoarthritis. Eur J Orthop Surg Traumatol Orthop Traumatol. Mai 2019;29(4):947–55.
- D’Ambrosi R, Mangiavini L, Loucas R, Loucas M, Brivio A, Mariani I, u. a. Similar rate of return to sports activity between posterior-stabilised and cruciate-retaining primary total knee arthroplasty in young and active patient. Knee Surg Sports Traumatol Arthrosc Off J ESSKA. Februar 2023;31(2):551–8.
- Overton C, Nelson AE, Neogi T. Osteoarthritis Treatment Guidelines from Six Professional Societies: Similarities and Differences. Rheum Dis Clin North Am. August 2022;48(3):637–57.
- Deutsche Gesellschaft für Orthopädie Und Unfallchirurgie e.V. Gonarthrose Version 4.0 vom 24.01.2024. 2024; Verfügbar unter: https://register.awmf.org/de/leitlinien/detail/033-004
- Phillips M, Bhandari M, Grant J, Bedi A, Trojian T, Johnson A, u. a. A Systematic Review of Current Clinical Practice Guidelines on Intra-articular Hyaluronic Acid, Corticosteroid, and Platelet-Rich Plasma Injection for Knee Osteoarthritis: An International Perspective. Orthop J Sports Med. 1. August 2021;9(8):23259671211030272.
- Conrozier T, Raman R, Diraçoglu D, Montfort J, Bard H, Baron D, u. a. EUROVISCO Consensus Guidelines for the Use of Hyaluronic Acid Viscosupplementation in Knee Osteoarthritis Based on Patient Characteristics. Cartilage. 20. November 2024;19476035241271970.
- Bannuru RR, Schmid CH, Kent DM, Vaysbrot EE, Wong JB, McAlindon TE. Comparative effectiveness of pharmacologic interventions for knee osteoarthritis: a systematic review and network meta-analysis. Ann Intern Med. 6. Januar 2015;162(1):46–54.
- Pereira TV, Jüni P, Saadat P, Xing D, Yao L, Bobos P, u. a. Viscosupplementation for knee osteoarthritis: systematic review and meta-analysis. BMJ. 6. Juli 2022;378:e069722.
- Migliorini F, Maffulli N, Schäfer L, Kubach J, Betsch M, Pasurka M. Less Pain with Intra-Articular Hyaluronic Acid Injections for Knee Osteoarthritis Compared to Placebo: A Systematic Review and Meta-Analysis of RandomisedControlled Trials. Pharm Basel Switz. 20. November 2024;17(11).
- Büchter R, Pieper D. Hyaluronsäure bei Kniearthrose – Sinvolle IGeL oder Placebo? Netzwerk für Evidenzbasierte Medizin. 2024;(06).
- Passi A, Vigetti D. Hyaluronan as tunable drug delivery system. Adv Drug Deliv Rev. Juni 2019;146:83–96.
- APTISSEN S.A. IFU Synolis 2020 [Internet]. Aptissen Webseite; 2020. Verfügbar unter: https://www.aptissen.com/wp-content/uploads/2023/02/PSL011-3-Leaftlet-February-2020.pdf
- APTISSEN S.A. Synolis VA Product Monograph [Internet]. Aptissen Webseite; o.J. Verfügbar unter: https://synolis.com/wp-content/uploads/2022/09/Aptissen-Monograph-V3.0.pdf
- Heisel J, Kipshoven C. Hyaluronic acid with sorbitol – efficacy and tolerability of intra-articular treatment for osteoarthritis of the knee. 2012; Verfügbar unter: DOI: 10.3238/oup.2012.0261-0266
- Athokpam A, HD V, Kalaiah K, Reddy P, Kiran S. Efficacy of intra-articular hyaluronic acid with sorbitol injection for pain relief in primary osteoarthritis knee. International Journal of Orthopaedics Sciences. 2024;10(4):170–9.
- Metsavaht L, Leporace G, Crespo B, Gonzalez F, Pereira MM, Guadagnin EC, u. a. Gait kinematics of osteoarthritic knees after intra-articular viscosupplementation: A double-blinded randomized controlled trial. The Knee. 1. März 2024;47:102–11.
Autoren
ist Facharzt für Orthopädie und Unfallchirurgie, Spezielle Unfallchirurgie und Sportmedizin. Er ist Gründer und Inhaber des LANS Medicum. Seine mannschaftsärztlichen Betreuungen umfassten u. a. das Handballteam des HSV sowie von 2011-2014 die Erstligafußballmannschaft des Hamburger SV. Heute betreut er mit seinem Team mehrere Fußball- und Hockeyteams sowie das Hamburger Ballett von John Neumeier. Außerdem ist Prof. Catalá-Lehnen als Professor für den Schwerpunkt Orthopädie an der Medical School Hamburg und am UKE in der Lehre für das Fach Knochenpathologie tätig.
ist Sportphysiotherapeutin und GCP-zertifizierte (AMG und MPDG) Studienkoordinatorin. Sie ist Head of Science am LANS Medicum Hamburg, studierte in Hamburg und Plymouth (UK) und schloss mit einem MSc Advanced Professional Practice in Physiotherapy mit dem Schwerpunkt Clinical Research ab.
Studium der Humanmedizin an der LMU München, Bern und VR China. Facharzt für Neurologie, spezielle Schmerztherapie und Rehabilitationswesen, Dozent und Ausbilder für Ärzte in der Schmerztherapie. Medizinischer Direktor für diverse Firmen.
© Andreas Kuhrau