Orthobiologika als innovative Behandlungsansätze für die regenerative /präventive Therapie und die Behandlung von Verletzungen haben in den vergangenen Jahren zu bedeutenden Fortschritten in der Sportmedizin geführt. Die minimal-invasiven Therapieoptionen aus organischen Materialien („natürliche biologische Substanzen“) dienen im orthopädischen Behandlungsspektrum der Funktionswiederherstellung und der Heilungsbeschleunigung [1 – 3].
Ein Anstieg der Publikationszahlen unterstreicht das wachsende Interesse sowie den Stellenwert von Orthobiologika in der Sportmedizin, insbesondere zur Beschleunigung der Therapie von überlastungsbedingten und degenerativen Schädigungen [4] (siehe dazu Artikel von Dr. Dr. Andreas Först „Orthobiologika“ in der sportärztezeitung 1/24). Zu den zurzeit verfügbaren Orthobiologika für typische orthopädische Pathologien zählen hyaluronic acid (HA), platelet-rich plasma (PRP), autologous conditioned serum (ACS) bzw. blood clot secretom (BCS), bone marrow aspirate concentrate (BMAC), bone marrow-derived stem cells (BMSCs), adipose-derived mesenchymal stem cells (AD-MSCs) und synthetic scaffolds sowie weitere für die Unfallchirurgie [5].
Mit einer weltweiten Prävalenz von 22,9 % (> 40-jährige) [6] und negativen Auswirkungen auf Lebensqualität und Aktivitäten des täglichen Lebens von Betroffenen führt Kniearthrose (knee osteoarthritis – Knie-OA) zu erheblichen sozialen Folgen und wirtschaftlichen Kosten [7]. Demzufolge sind neue präventive und konservative Therapieoptionen und Behandlungsansätze, gerade im Bereich der Sportmedizin, auch zukünftig von großer Bedeutung. Vorteile von Orthobiologika sind neben dem großen Therapiepotenzial auch die minimale Invasivität und die „überschaubaren“ Kosten im Vergleich zu operativen Therapien [8].
Aktuelles aus der Leitlinie
Die S2k-Gonarthrose Living Guideline der Deutschen Gesellschaft für Orthopädie und Unfallchirurgie e. V. empfiehlt im Rahmen der konservativen Therapie von Knie-OA primär Kraft-, Ausdauer- und Beweglichkeitstraining. Als Injektionen können laut 2024 aktualisierter Empfehlung intraartikulär applizierte Corticosteroide kurzzeitig für die Therapie von schmerzhafter Gonarthrose erwogen werden, wenn diese möglichst niedrig, aber wirksam dosiert sind und die Applikation leitliniengerecht durchgeführt wird [9]. Corticosteroidinjektionen sollten angesichts der aktuell vorliegenden Hinweise auf erhebliche Nebenwirkungen, wie z. B. die Hemmung des Knorpelstoffwechsels und Reduktion der Knorpelmasse sorgfältig abgewogen werden (siehe dazu Artikel von Prof. Dr. Götz Welsch „Update Intraartikuläre Injektionen: Eine aktuelle Literatur-Übersicht“ in der sportärztezeitung 4/23) [10 – 12]. Nebenwirkungen lassen sich in lokale und systemische sowie sofortige und verzögert auftretende Nebenwirkungen einteilen, die von der Zielgruppe abhängig sein können (z. B. Sportler) und demzufolge individuell betrachtet werden sollten [13]. Intraartikuläre HA-Injektionen hingegen können bei Patienten erwogen werden, bei denen der Einsatz von NSAR kontraindiziert oder nicht ausreichend wirksam ist. Für ein bestimmtes Herstellungsverfahren von PRP kann derzeit keine Empfehlung gegeben werden [9].
Zurzeit wird vermehrt die Applikation von Kollagen bei verschiedenen Erkrankungen des muskuloskelettalen-Systems diskutiert, z. B. konnten bei Patienten mit Knie-OA bereits erste positive Outcomes berichtet werden [14 – 19]. In einem aktuellen RCT führten hydrolysierte Kollagenpeptide bei Patienten mit Seitenbandschmerzen am Knie im Vergleich zur Kontrollgruppe, die orale Schmerzmedikation und eine Corticosteroidinjektion erhielt, zu einer Schmerzlinderung und Verbesserung des funktionellen Status und der Lebensqualität, ohne Intergruppenunterschiede. Die Interventionsgruppe gab eine höhere Zufriedenheit an und es wurden keine unerwünschten Ereignisse dokumentiert. Demzufolge könnte Kollagen eine vielversprechende Behandlungsalternative und/oder Ergänzung darstellen und möglicherweise Nebenwirkungen von Corticosteroidinjektionen umgehen [20].
Kollagen
Kollagen ist ein grundlegendes Strukturelement des Bindegewebes (organisch: Knochen, Zähne, Knorpel, Sehnen, Bänder) und macht bei Menschen > 30 % des Gesamtproteins aus [21 – 23]. Insgesamt werden 28 verschiedene Arten von Kollagen unterschieden, bei denen einige Funktionen noch unklar sind [24]:
- Kollagen Typ I – faserbildend in Kollagenfasern: Haut, Sehnen, Knochen, Dentin, Faserknorpel, Hornhaut
- Kollagen Typ II – faserbildend: hyaliner und elastischer Knorpel, Glaskörper
- Kollagen Typ III – faserbildend in Retikulinfasern: Haut, Skelettmuskulatur, Blutgefäße
Kollagen besteht strukturell aus drei langen, linkshändigen Aminosäureketten (zwei identische α1-Ketten und eine α2-Kette), die zu einer kompakten rechtshändigen Dreifachhelix gewickelt sind [25]. Durch enzymatische Hydrolyse wird Kollagen in kleinere Peptide aufgespalten, wodurch die Bioverfügbarkeit und Absorption im Körper beeinflusst werden. Durch das Molekulargewicht von < 3.000 Daltons weisen Kollagenpeptide eine hohe Biokompatibilität auf [26, 27]. Die Wirkweise von Kollagen basiert auf komplexen Mechanismen, die noch nicht im Detail nachvollzogen sind und weiter klinisch geprüft werden müssen [15].
Vorsichtige positive Befunde weisen auf einen Nutzen der Einnahme von Kollagenpräparaten (Typ II nativ oder hydrolysat) bei Arthrose hin (siehe dazu Artikel von Prof. Dr. Nadine Berling und Ronny Heldt-Döpel „Kollagene im Sport: Arthroseprävention und -therapie“ in der sportärztezeitung 3/23) [26]. Durch Kollagensupplementation konnten in einzelnen Tier- und Humanstudien erste Hinweise auf eine Zunahme der Mineralmasse und Knochendichte und Hemmung entzündlicher Zytokine dokumentiert werden [28]. Lin et al. (2023) fanden in ihrer Übersichtsarbeit eine signifikante Schmerzreduktion bei Patienten mit Knie-OA nach Supplementation von Kollagenpeptiden. Die Aussagekraft der Ergebnisse ist jedoch aufgrund möglicher Verzerrungen, kleiner Stichproben und Inkonsistenzen innerhalb der eingeschlossenen Studien begrenzt. Die Vertrauenswürdigkeit in den Effektschätzer für das Outcome Schmerz mittels GRADE-Beurteilung wird als moderat und für „adverse effects“ als sehr niedrig eingestuft [29].
Eine andere klinische Anwendung von Kollagen ist über lokale Injektionen möglich, die bei verschiedenen Erkrankungen des Muskuloskelettalen-Systems bereits positive Outcomes gezeigt hat, z. B. bei Patienten mit Knie-OA [14 – 19] und Sehnenentzündungen [30]. Tarantino et al. (2023) ordnen die intraartikuläre Verabreichung von Typ-I-Kollagen, basierend auf den Ergebnissen von sieben Studien, als wirksam zur Symptomreduktion und Verbesserung der Funktionsfähigkeit bei Knie-OA ein. Während z. T. keine Nebenwirkungen auftraten, wurden in anderen Studien moderate Reaktionen auf die Injektionen und Schmerzen an den Injektionsstellen berichtet. Zur Bestätigung der Ergebnisse wird sich für Langzeiterhebungen und weitere in-vitro- und in-vivo-Forschung ausgesprochen, damit die Auswirkungen von Typ-I-Kollagen als intraartikuläre Behandlung für Knie-OA noch umfassender nachvollzogen werden können [31]. Durch Verzerrungsrisiken der Einzelstudien sollten die Ergebnisse kritisch hinterfragt und stets in die gesamte Fachliteratur eingeordnet werden.
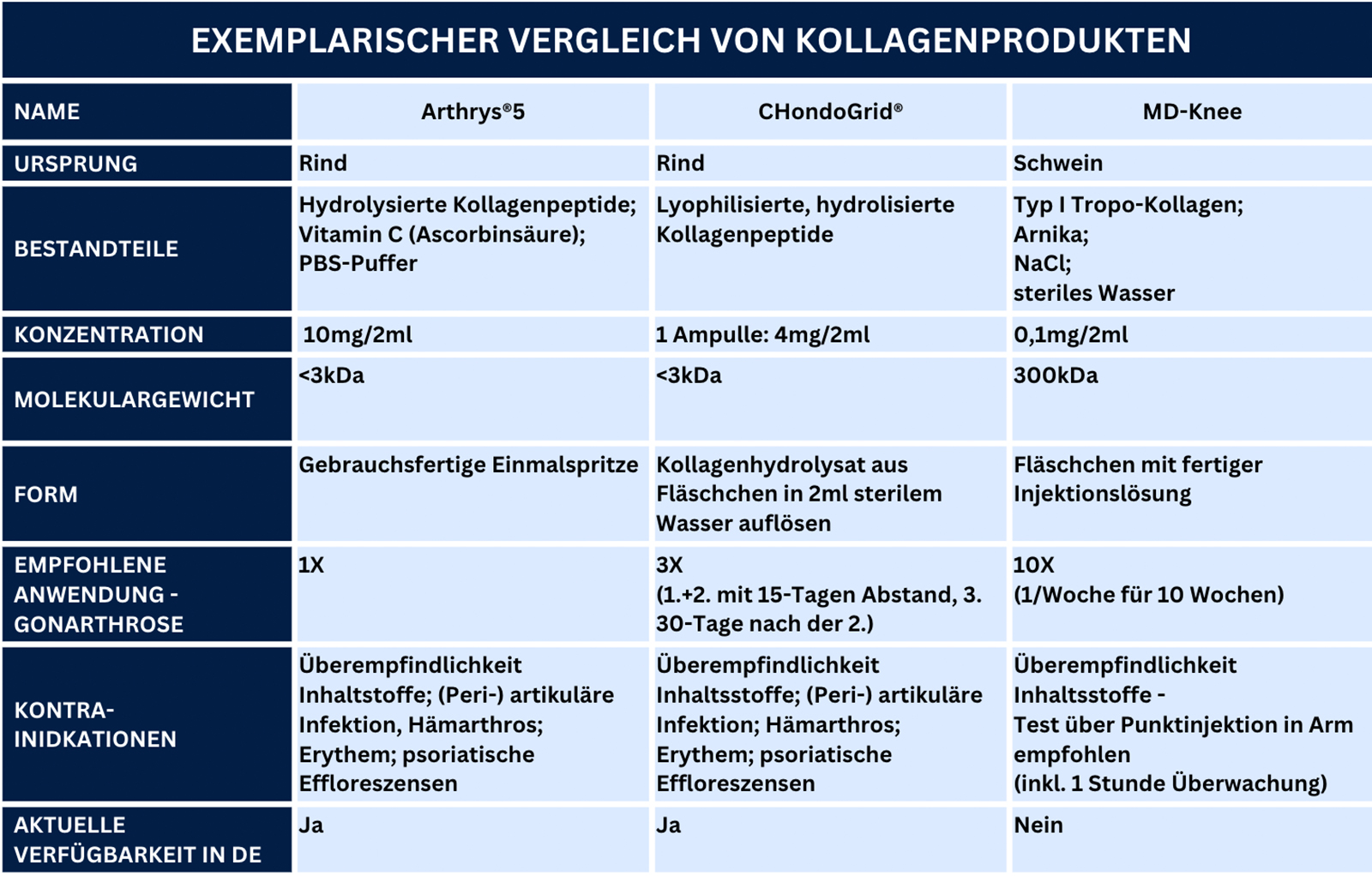
Exemplarischer Vergleich von Kollagenprodukten
Die Tabelle zeigt einen exemplarischen Vergleich von Kollagenprodukten für die Anwendung am muskuloskelettalen-System am Beispiel intraartikulärer Injektionen. Die Hersteller bieten z. T. auch weitere Produkte in angepassten Zusammensetzungen für andere Indikationen an. Der Fokus liegt auf den Produkten Arthrys®5, CHondroGrid® und MD-Knee aufgrund der Verfügbarkeit von Informationen, gleichwohl in einer aktuellen Übersichtsarbeit noch weitere Produkte wie z. B. Cartifill, CartiZol und Fibroquel aufgeführt wurden [23]. Die Tabelle zeigt Unterschiede zwischen den verfügbaren Produkten für intraartikuläre Injektionen, z. B. bezüglich des Ursprungs (Rind / Schwein) und der Molekulargewichte (< 3 kDa / 300 kDa). Während Arthrys®5 und MD-Knee gebrauchsfertig sind, muss CHondroGrid® vor Verabreichung mit sterilem Wasser für Injektionen angemischt werden. Vor der jeweiligen Applikation sind zwingend die individuellen Herstellerangaben der Produkte zu beachten. Eine umfassende Vorbereitung der Applikation von Orthobiologika und hygienisch korrektes Arbeiten unter aseptischen Bedingungen sind zur Minimierung des Komplikationsrisikos und der Infektionsgefahr obligat (Beachte: Herstellerangaben, Hygieneleitlinien zu Punktion und Injektion der KRINKO und S-1 Leitlinie Intraartikuläre Punktionen und Injektionen: Hygienemaßnahmen – in Überarbeitung, AWMF) [2, 32, 33].
Case-Report: Knorpelschaden Kniegelenk
Erste Erfahrungen aus der praktischen Anwendung von intraartikulären Kollageninjektionen aus der sportmedizinischen Praxis. Wiedervorstellung eines 60-jährigen männlichen Patienten (ehemaliger Profisportler) mit symptomatischer Knie-OA und Knorpelschaden (femoropatellar III° – IV°). Der Patient stellte sich ursprünglich mit starken Schmerzen im Knie (VAS 6 – 7 / 10) nach längeren Gehstrecken (> 3 km) vor und war in seinen Alltagsaktivitäten stark eingeschränkt. Nach einer umfassenden initialen Diagnostik begann der Patient mit einer intensiven medizinischen Trainingstherapie zur Verbesserung der muskulären Stabilisierung des Kniegelenks (personal Training durch Sportwissenschaftler – supervisiertes Training empfohlen AAOS – Guideline 2021). Eine adjuvante Therapie mit intraartikulären Injektionen zur Verbesserung der Beweglichkeit und Gelenkfunktion, Schmerzlinderung und Regenerationsförderung komplettierte das Therapiekonzept.
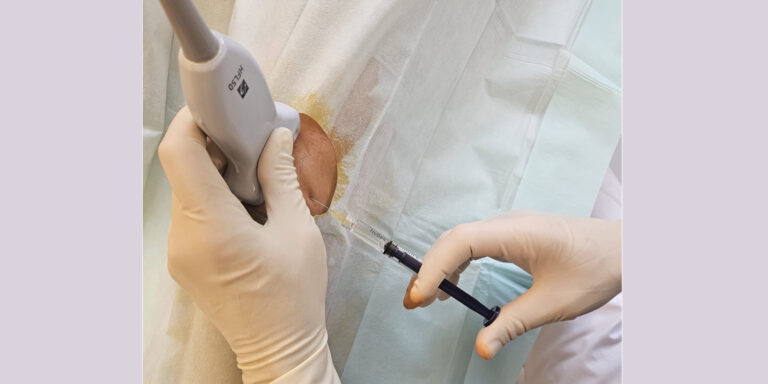
- Tag 0: (Diagnostik: Gelenkentzündung -> Aspiration der Synovialflüssigkeit); 1 intraartikuläre HA-Injektion (mit hohem Molekulargewicht) unter sonografischer Kontrolle
- Tag 7: 1 intraartikuläre HA-Injektion (hohes Molekulargewicht) unter sonografischer Kontrolle
- Tag 14: (Diagnostik: keine Gelenkentzündung oder Gelenkerguss); 1 intraartikuläre PRP-Injektion (leukozytenarm) unter sonografischer Kontrolle
Dem ersten Behandlungszyklus folgend verbesserte sich die Lebensqualität des Patienten durch eine deutliche Schmerzreduktion bei längeren Gehstrecken.Die Wiedervorstellung des Patienten folgte einem Wanderurlaub aufgrund von lokalen Schmerzen hinter der Patella, woraufhin dem Patienten alternative Behandlungsoptionen vorgestellt wurden.
- Tag 28: (Diagnostik: keine Gelenkentzündung oder Gelenkerguss); 1 intraartikuläre Injektion von Kollagen unter sonografischer Kontrolle
Der Patient erhielt eine intraartikuläre Injektion von Arthrys® 5 mg / 2 ml. Drei Tage später berichtete der Patient von einer deutlichen Schmerzreduktion beim Gehen (VAS 2 / 10) und konnte seinen normalen Alltagsaktivitäten wieder gewohnt nachkommen. Dieser Zustand konnte für drei Monate aufrecht gehalten werden.
Fazit
Orthobiologische Kombinationstherapien zeigen vielversprechende Ergebnisse für patientenrelevante klinische Outcomes. Auf Basis der angenommenen Wirkmechanismen und der klinischen Erfahrungen werden zurzeit unterschiedliche Behandlungsalgorithmen entwickelt, mit dem Ziel, potenzielle Therapiesynergismen möglichst effektiv nutzbar zu machen.
Die Herausforderung bei der (Weiter-) Entwicklung von Kombinationstherapien in der Sportmedizin besteht darin, indikationsspezifisch optimale Kombinationen mit den verfügbaren Produkten zu ermitteln und die potenziellen Effekte zu evaluieren. Dafür sind randomisierte kontrollierte Studien unter standardisierten Bedingungen obligat. Behandlungsoptionen sollten daher zwingend individuell abgewägt und kritisch analysiert werden. Klinisch Tätige sollten sich fortlaufend über die aktuellsten Forschungsergebnisse und evidenzbasierten Empfehlungen informieren.
Literatur
- Makaram NS, Safran MR, Abrams GD, Sherman SL, Murray IR. Rationale for the Use of Orthobiologics in Sports Medicine. Oper Tech Sports Med. 1. September 2020;28(3):150753.
- Moreno-Garcia A, Rodriguez-Merchan EC. Orthobiologics: Current role in Orthopedic Surgery and Traumatology. Arch Bone Jt Surg. Juli 2022;10(7):536–42.
- Angele P, Buchhorn T, Zellner J. Orthobiologics in der klinischen Anwendung. Thema Neuer Kniechirurgie Innov Knee Surg. 1. Dezember 2022;38(4):424–30.
- Obana KK, Schallmo MS, Hong IS, Ahmad CS, Moorman CT 3rd, Trofa DP, u. a. Current Trends in Orthobiologics: An 11-Year Review of the Orthopaedic Literature. Am J Sports Med. September 2022;50(11):3121–9.
- Mavrogenis AF, Karampikas V, Zikopoulos A, Sioutis S, Mastrokalos D, Koulalis D, u. a. Orthobiologics: a review. Int Orthop. Juli 2023;47(7):1645–62.
- Cui A, Li H, Wang D, Zhong J, Chen Y, Lu H. Global, regional prevalence, incidence and risk factors of knee osteoarthritis in population-based studies. EClinicalMedicine. Dezember 2020;29–30:100587.
- Xie F, Kovic B, Jin X, He X, Wang M, Silvestre C. Economic and Humanistic Burden of Osteoarthritis: A Systematic Review of Large Sample Studies. PharmacoEconomics. November 2016;34(11):1087–100.
- Hussain ZB, Chahla J, LaPrade RF, Mandelbaum BR. Orthobiologics: Today and Tomorrow. In: Farr J, Gomoll AH, Herausgeber. Cartilage Restoration: Practical Clinical Applications [Internet]. Cham: Springer International Publishing; 2018. S. 131–42. Verfügbar unter: https://doi.org/10.1007/978-3-319-77152-6_11
- DGOU. Gonarthrose (Living Guideline) S2k-Leitlinie – Deutsche Gesellschaft für Orthopädie und Unfallchirurgie e.V. 29. Februar 2024; Verfügbar unter: https://register.awmf.org/de/leitlinien/detail/033-004
- Kompel AJ, Roemer FW, Murakami AM, Diaz LE, Crema MD, Guermazi A. Intra-articular Corticosteroid Injections in the Hip and Knee: Perhaps Not as Safe as We Thought? Dezember 2019;293(3).
- Hirsch G, Kitas G, Klocke R. Intra-articular corticosteroid injection in osteoarthritis of the knee and hip: factors predicting pain relief–a systematic review. Semin Arthritis Rheum. April 2013;42(5):451–73.
- McAlindon TE, LaValley MP, Harvey WF, Price LL, Driban JB, Zhang M, u. a. Effect of Intra-articular Triamcinolone vs Saline on Knee Cartilage Volume and Pain in Patients With Knee Osteoarthritis: A Randomized Clinical Trial. JAMA. 16. Mai 2017;317(19):1967–75.
- Kamel SI, Rosas HG, Gorbachova T. Local and Systemic Side Effects of Corticosteroid Injections for Musculoskeletal Indications. AJR Am J Roentgenol. März 2024;222(3):e2330458.
- De Luca P, Colombini A, Carimati G, Beggio M, de Girolamo L, Volpi P. Intra-Articular Injection of Hydrolyzed Collagen to Treat Symptoms of Knee Osteoarthritis. A Functional In Vitro Investigation and a Pilot RetrospectiveClinical Study. J Clin Med. 4. Juli 2019;8(7).
- Volpi P, Zini R, Erschbaumer F, Beggio M, Busilacchi A, Carimati G. Effectiveness of a novel hydrolyzed collagen formulation in treating patients with symptomatic knee osteoarthritis: a multicentric retrospective clinicalstudy. Int Orthop. Februar 2021;45(2):375–80.
- Furuzawa-Carballeda J, Lima G, Llorente L, Nuñez-Álvarez C, Ruiz-Ordaz BH, Echevarría-Zuno S, u. a. Polymerized-type I collagen downregulates inflammation and improves clinical outcomes in patients with symptomatic knee osteoarthritis following arthroscopiclavage: a randomized, double-blind, and placebo-controlled clinical trial. ScientificWorldJournal. 2012;2012:342854.
- Martin Martin LS, Massafra U, Bizzi E, Migliore A. A double blind randomized active-controlled clinical trial on the intra-articular use of Md-Knee versus sodium hyaluronate in patients with knee osteoarthritis(„Joint“). BMC Musculoskelet Disord. 22. Februar 2016;17:94.
- Reshkova V, Rashkov R, Nestorova R. EFFICACY AND SAFETY EVALUATION OF GUNA COLLAGEN MDs INJECTIONS IN KNEE OSTEOARTHRITIS − A CASE SERIES OF 30 PATIENTS. Physiological Regulating Medicine. 2016;27–9.
- Lee HS, Oh KJ, Moon YW, In Y, Lee HJ, Kwon SY. Intra-articular Injection of Type I Atelocollagen to Alleviate Knee Pain: A Double-Blind, Randomized Controlled Trial. Cartilage. Dezember 2021;13(1_suppl):342S-350S.
- Luu Thi B, Tran Thi L, Hang Hoang Thi M. Effectiveness of Hydrolyzed Collagen Peptide Injection for the Treatment of Collateral Ligament Pain: A Randomized Controlled Trial. Journal of Clinical & Medical Surgery. 2023;3(2).
- Gallo N, Natali ML, Sannino A, Salvatore L. An Overview of the Use of Equine Collagen as Emerging Material for Biomedical Applications. J Funct Biomater. 1. November 2020;11(4).
- Salvatore L, Gallo N, Natali ML, Terzi A, Sannino A, Madaghiele M. Mimicking the Hierarchical Organization of Natural Collagen: Toward the Development of Ideal Scaffolding Material for Tissue Regeneration. Front Bioeng Biotechnol. 2021;9:644595.
- Salvatore L, Natali ML, Brunetti C, Sannino A, Gallo N. An Update on the Clinical Efficacy and Safety of Collagen Injectables for Aesthetic and Regenerative Medicine Applications. Polymers. 17. Februar 2023;15(4).
- Wang H. A Review of the Effects of Collagen Treatment in Clinical Studies. Polymers. 9. November 2021;13(22).
- Sorushanova A, Delgado LM, Wu ZN, Shologu N, Kshirsagar A, Raghunath R, u. a. The Collagen Suprafamily: From Biosynthesis to Advanced Biomaterial Development. Advanced Materials. 2019;(31):1–39.
- Martínez-Puig D, Costa-Larrión E, Rubio-Rodríguez N, Gálvez-Martín P. Collagen Supplementation for Joint Health: The Link between Composition and Scientific Knowledge. Nutrients [Internet]. 2023;15(6). Verfügbar unter: https://www.mdpi.com/2072-6643/15/6/1332
- Elango J, Hou C, Bao B, Wang S, Maté Sánchez de Val JE, Wenhui W. The Molecular Interaction of Collagen with Cell Receptors for Biological Function. Polymers. 23. Februar 2022;14(5).
- Campos LD, Santos Junior V de A, Pimentel JD, Carregã GLF, Cazarin CBB. Collagen supplementation in skin and orthopedic diseases: A review of the literature. Heliyon. April 2023;9(4):e14961.
- Lin CR, Tsai SHL, Huang KY, Tsai PA, Chou H, Chang SH. Analgesic efficacy of collagen peptide in knee osteoarthritis: a meta-analysis of randomized controlled trials. J Orthop Surg. 16. September 2023;18(1):694.
- Uroz NZ. COLLAGEN MEDICAL DEVICE INFILTRATIONS IN SHOULDER PATHOLOGIES. CALCIFIC SUPRASPINATUS TENDINITIS. Physiological Regulating Medicine. 2016;15–7.
- Tarantino D, Mottola R, Palermi S, Sirico F, Corrado B, Gnasso R. Intra-Articular Collagen Injections for Osteoarthritis: A Narrative Review. Int J Environ Res Public Health. 1. März 2023;20(5).
- Labmayr V, Eckhart FJ, Smolle M, Klim S, Fischerauer SF, Bernhardt G, u. a. Sterile Punktion großer Gelenke. Oper Orthop Traumatol. 1. Februar 2023;35(1):65–80.
- Infektionsprävention (KRINKO). Kommentar zur Empfehlung „Anforderungen an die Hygiene bei Punktionen und Injektionen“. Robert Koch-Institut; 2021. S. 13–15.
- TISS’YOU S.r.l. Arthrys – Regenerative peptides [Internet]. TISS’YOU S.r.l; Verfügbar unter: https://www.tissyou.com/wp-content/uploads/2020/11/Arthrys_brochure_web_pagine-singole-ENG.pdf
- Bioteck S.p.A. CHondroGrid – The new collagen way. Innovative und progressive Behandlungsmethode bei Chondropathie. Produktinformation SpongioTech; o.A..
- Guna S.p.a. Manual of Injection Therapy for the Musculoskeletal System. 2022.
Autoren
ist Facharzt für Orthopädie und Unfallchirurgie, Spezielle Unfallchirurgie und Sportmedizin. Er ist Gründer und Inhaber des LANS Medicum. Seine mannschaftsärztlichen Betreuungen umfassten u. a. das Handballteam des HSV sowie von 2011-2014 die Erstligafußballmannschaft des Hamburger SV. Heute betreut er mit seinem Team mehrere Fußball- und Hockeyteams sowie das Hamburger Ballett von John Neumeier. Außerdem ist Prof. Catalá-Lehnen als Professor für den Schwerpunkt Orthopädie an der Medical School Hamburg und am UKE in der Lehre für das Fach Knochenpathologie tätig.
ist Sportphysiotherapeutin und GCP-zertifizierte (AMG und MPDG) Studienkoordinatorin. Sie ist Head of Science am LANS Medicum Hamburg, studierte in Hamburg und Plymouth (UK) und schloss mit einem MSc Advanced Professional Practice in Physiotherapy mit dem Schwerpunkt Clinical Research ab.