Am 12. Juni 2016 rechnet Liverpools Ex-Spieler Daniel Agger mit seinem Verein und den Ärzten ab. Agger, der von 2006 bis 2014 für die Reds in der englischen Premier League aktiv war, sagte: „Ich habe zu viele Schmerzmittel in meiner Karriere genommen. Das weiß ich genau und das ist schlecht. Aber ich habe damit aufgehört.“ Agger, der zuletzt beim dänischen Klub Bröndby IF spielte, zog sich nach der zurückliegenden Saison aus gesundheitlichen Gründen zurück. Laut dem Bericht hätten die Teamärzte in Liverpool die Einnahme der Medikamente gesteuert. Wann immer Agger sich weigerte, die schmerzstillenden Mittel einzunehmen, sei er dazu gezwungen worden.
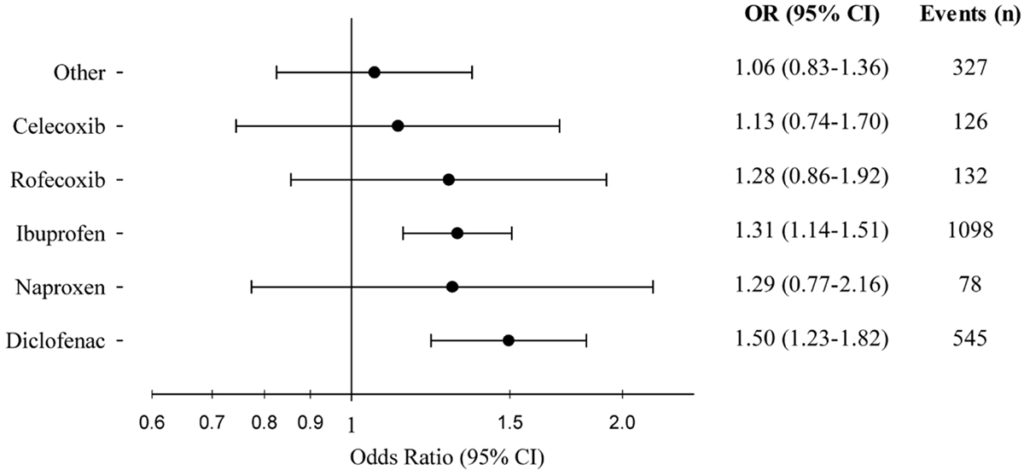
Im März 2017 werden zwei Mannschaftsärzte eines Erstligisten der Fußball Bundesliga durch das Landgericht Bremen in einem Grundsatz- und Teilurteil zu einer Zahlung von 100.000 Euro Schmerzensgeld verurteilt. Der 37-Jährige Spieler habe wegen „mehrerer Behandlungsfehler“, u. a. der Gabe von Diclofenac, seine Niere verloren. Auch die Behandlungskosten und sein Verdienstausfall im Jahre 2007 in Millionenhöhe sollen ausgeglichen werden. 2017 veröffentlichen Sondergaard und Gislason ein deutlich erhöhtes Herzstillstandrisiko unter verschiedenen NSAR. Bezogen auf die einzelnen Substanzen ist die Herzstillstandrate nach den Berechnungen für Diclofenac um 50 % und unter Ibuprofen um 31% erhöht (Abb.1).
Einsatz von NSAR
Seit 1970 werden entzündliche Erkrankungen und viele akute Verletzungen traditionell mit NSAR behandelt. Dennoch haben sich diese Substanzen vor allem bei chronischer Anwendung als schädlich mit unerwünschten Nebenwirkungen gezeigt. Zudem werden sie auch bei manchen Erkrankungen als ineffektiv erachtet (García-Lafuente 2009; Page 2000). NSAR können die frühentzündliche Reaktion im geschädigten Areal und damit die anschließend sekundär schädigende Wirkung verhindern. So werden zur Prävention der heterotropen Ossifikation nach Totalendoprothese des Hüftgelenkes NSAR für 7 Tage empfohlen (Kölbl et al. 2003). Auch gilt die Empfehlung, NSAR nur in den ersten 2–3 Tagen bei Muskelverletzungen zu geben (Müller-Wohlfahrt, H.W., Ueblacker, P. & Hänsel L., 2010).
Negative Auswirkungen auf den Muskel-Sehnenapparat und damit auf die Regeneration
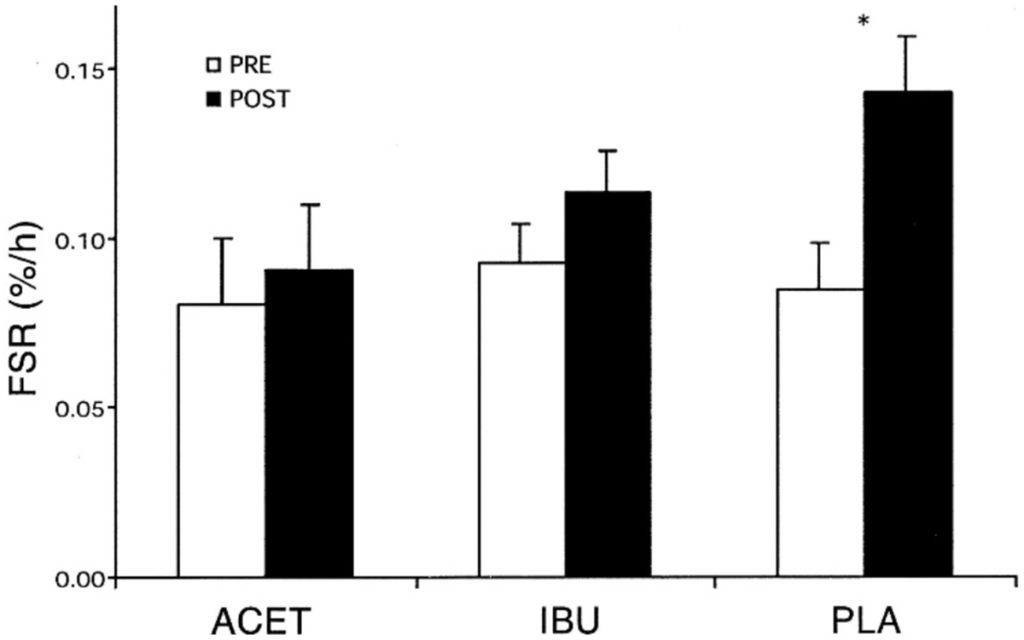
Im Rahmen der Regeneration und der Remodellierung des Muskelsehnenapparates wird im Leistungssport eine qualitativ hochwertige Eiweißzufuhr von mindestens 2 g / kg / KG angestrebt und im Trainingsprozess insbesondere die Gabe nach Belastung, um die Proteinbiosynthese optimal zu stimulieren. NSAR zeigen einen deutlich negativen Effekt auf die Regeneration, indem sie Proteinbiosynthese hemmen. Trappe et al. konnten 2002 zeigen, wie nach Einnahme von 1200 mg Ibuprofen innerhalb von 24h nach Krafttraining die fibrilläre Syntheserate ebenso wie bei Acetaminophen (Paracetamol; Gruppe der Nichtopioid-Analgetika) deutlich geringer anstieg, also im Vergleich zu Placebo unterdrückt wurde (Abb. 2).
Forslund (2003) fand unter NSAR einen verringerten Querschnitt und Kollagengehalt in heilenden Sehnen. Cohen et al. (2006) fand zu jedem Zeitpunkt signifikante Unterschiede in der Belastbarkeit, Kollagenorganisation und Reifung des Sehnenapparates in der Celecoxib und Indometacin Gruppe nach Rotatorenmanschettenruptur bei Ratten. Auch Paracetamol (Acetaminophen, APAP) verändert die Prostaglandin-Produktion im Skelettmuskel des Menschen und die Rezeptorexpression (Trappe et al. 2001,2013), was die Kollagenbildung beeinflussen kann (Kjaer, 2004). Kollagenfibrillen sind durch Hydroxylyslpyridinolin (HP) und Lysylpyridinolin (LP) vernetzt, die primären Bestandteile der extrazellulären Matrix (ECM). Die Anzahl von Kollagenfibrillen und Vernetzungsgrad beeinflussen die Zugfestigkeit und Steifigkeit der Gewebe. Paracetamol induziert eine Verringerung der Vernetzung und kann zur Verringerung der Sehnensteifigkeit führen. Tsai et al. (2010) stellten fest, dass Ibuprofen die Expression von Kollagenasen einschließlich MMP-1, -8, -9 und -13 hochreguliert, ohne die Expression von Collagen vom Typ I und III zu beeinflussen. Diese Ergebnisse deuten auf einen molekularen Mechanismus hin, der möglicherweise die Hemmung der Sehnenheilung durch Ibuprofen erklärt. Ebenso hemmen selektive COX-2-Inhibitoren die Sehnenheilung signifikant (Lu et.al 2015).
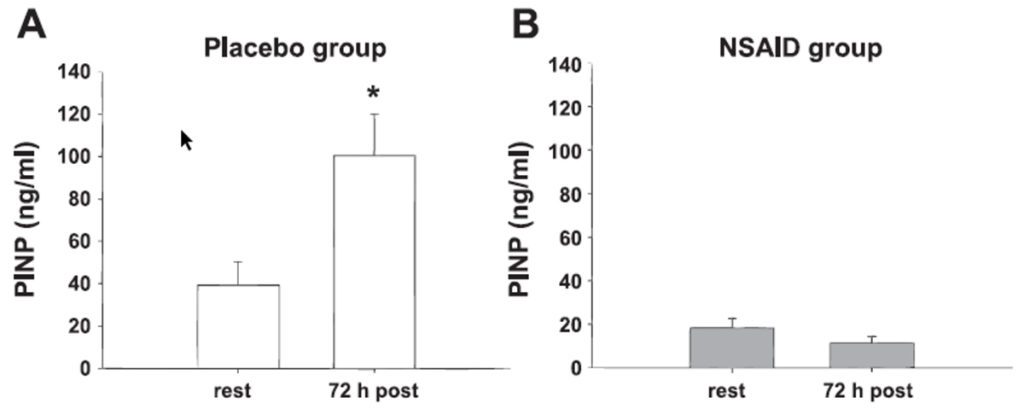
Britt et al. (2011) zeigten bei Einnahme von Indometacin für 7 Tage den Effekt einer PGE2 Blockade durch NSAR in der Patellarsehne vor und 72 Stunden nach einem 36 km Lauf. Deutlich sichtbar am Propeptid des Typ I Prokollagens (PINP) (Abb. 3).
Auch die Sehnen-zu-Knochen-Heilung wird bei Rekonstruktion des vorderen Kreuzbandes reduziert. So nahm unter COX-2 Hemmung die Stabilität des Kreuzbandtransplantats ab und war im Vergleich zu den Kontrollen um 37 % reduziert (Sauerschnig et al. 2018). Einige Studien liefern Hinweise, dass der Gebrauch von NSAR bei Muskelverletzungen mit einer erhöhten Fibroserate der betroffenen Muskelpartie einhergeht (Paoloni et al. 2009; Ziltener et al. 2010). Weiterhin können durch die analgetische Komponente protektive Schmerzreize maskiert werden, die bei betroffenen Sportlern zu einer zu frühen Belastungssteigerung und damit mit der Gefahr einer Rezidiv-Verletzung einhergehen können. Werden diese Medikamente während des Trainings eingenommen, können sie die Sehnenanpassungen (erhöhte Steifheit und verringerte Dehnung) verändern und letztendlich die Verbesserung der körperlichen Funktion einschränken. Dies ist auch wichtig für ältere Menschen, die ermutigt werden sollen, Sport zu treiben, um Gesundheit und Muskelmasse zu verbessern und täglich COX-hemmende Medikamente einnehmen. Da die Alterung selbst zu einer Veränderung der extrazellulären Matrixstruktur und einer regionspezifischen Abnahme der Größe und Signalintensität z.B. der Patellarsehne führt, könnte der Konsum von COX-hemmenden Arzneimitteln diesen Prozess verstärken. Ältere sollen im Gegensatz zu jungen Menschen mehr Eiweiß zuführen, um die Proteinbiosynthese optimal zu stimulieren, die allerdings auch wie oben beschrieben durch NSAR gehemmt wird. Lange ist bekannt, dass die Gabe von NSAR die Frakturheilung verlangsamt (Beck et al.2003; Simon et al. 2007) und zu einer erhöhten Rate von Pseudarthrosen führt (Giannoudis et al. 2000).
Auch die hormonelle Seite ist von NSAR nicht unbeeinflusst. So zeigten Kristensen et al. (2018) in einer aktuellen Studie, dass Ibuprofen bei 31 gesunden jungen Männern zwischen 18 und 35 Jahren die Testosteronproduktion in den Hoden bei Einnahme von Ibuprofen (2 x 600 mg / d) über sechs Wochen hemmte und damit zu einem kompensierten Hypogonadismus wie bei älteren Männern führte. Der Heilungsprozess bei Muskelverletzungen erfolgt durch die Produktion von Zytokinen, Wachstumsfaktoren und Sauerstoff-Radikalen der Makrophagen wobei Satelliten-Zellen am Tage 3–5 mobilisiert und zur Proliferation angeregt werden um dann mit den Myozyten fusionieren. Während Mehallo (2006) einen kurzzeitigen Einsatz von NSAR innerhalb der ersten 5–7 Tage nach Verletzung überwiegend positiv beschreiben, kommen Järvinen et al. (2013) zu einer Empfehlung nur noch für die ersten 2–3 Tage aufgrund der Blockierung der Entzündung im Akutstadium und der Aktivierung von Satellitenzellen. Eine placebokontrollierte experimentelle Studie konnte unter der Anwendung von Ibuprofen (1200 mg / d) bei exzentrischer Muskelbelastung des M. vastus lateralis, hervorgerufen durch eine elektrische Muskelstimulation, eine gesteigerte Satellitenzellproliferation in der regeneratorischen Frühphase aufzeigen (Mackey et al. 2016). Schlussfolgernd könnte die Anwendung von Ibuprofen zwischen 48–96 Stunden posttraumatisch mit positiv therapeutischen Effekten einhergehen.
Ob pflanzliche entzündungshemmende Substanzen einen gleichen Effekt haben, um die anderen Nebenwirkungen zu vermeiden, wäre zu untersuchen. Letztlich sollte die Indikation zur Ein-
nahme von NSAR bei Muskelverletzungen streng gestellt werden. Die off-label-Anwendung von Indometacin zur Prophylaxe einer Myositis ossificans kann bei höhergradigen Verletzungen (z. B. Typ IIIb-IVb) mit sonografischem Hinweis auf eine beginnende Ossifikation zu rechtfertigen sein.
Alternative natürliche Nahrungsquellen?
Konsequenterweise ist der Fokus auf natürliche Nahrungsquellen als Alternative zu den synthetischen NSAR Behandlungen geschwenkt. Im Sport kommt es durch Verletzungen, Überlastungen und extrem hohen physischen Belastungen durch Antritte und Abbrems-, Sprung und Rotationsbewegungen sowie durch Kontusionen in Kontaktsportarten zu ständigen entzündlichen Veränderungen. Es ist bekannt, dass Ernährung an sich wie über Arachidonsäure oder gebildete Harnsäure zusätzlich entzündlich wirken kann. Purine und Fruktose fördern die Bildung von Harnsäure.
Ernährung kann aber auch stark entzündungshemmend wirken und somit nicht nur die Regeneration beschleunigen und präventiv wirken, sondern auch Medikamente, welche regenerationshemmend wirken und viele unerwünschten Nebenwirkungen haben, ersetzen. Hierzu wurden insbesondere pflanzliche Inhaltsstoffe und Enzyme untersucht, die sich adäquat dosiert z. B. auch als Nahrungsergänzungsmittel eignen. Enzyme wie Bromelain aus der Ananas, sind bereits lange im Sportbereich bekannt und brauchen den Vergleich der Wirksamkeit zu COX-hemmenden Arzneimitteln als sogenannte „natürliche“ Arzneimittel nicht zu scheuen. So zeigte sich eine Enzymkombination mit Bromelain in einer gepoolten Meta-Analyse basierend auf individuellen Patientendaten von sechs randomisierten Studien genauso effektiv (Überall et al. 2016). Weitere interessante Substanzen sind, wie im IOC Konsensuspapier kürzlich (Maughan et al. 2018) und Consensus Statement 2019 der International Association of Athletics Federations veröffentlicht, Omega 3 Fettsäuren und Vitamin D. Kurkumin und Boswellia serrata weisen ebenfalls antiinflammatorische Kapazitäten auf, die bei Athleten untersucht wurden (z. B. Chilelli et al. 2016). Ebenso haben die Inhaltsstoffe der roten Beete und die Anthocyanine der Sauerkirsche stark entzündungshemmende Wirkung (Bondesen et al. 2004). Beeren haben TNF-a induzierte Hochregulation von Entzündungsmediatoren in menschliche mikrovaskuläre Endothelzellen reduziert (Youdim et al. 2002). Regenerationsunterstützung und Entzündungshemmung ist also ohne weiteres durch natürliche Substanzen möglich, die genannte negative Effekte der NSAR Behandlung nicht aufzeigen.
Nehrer S., Valderrabano V. und Engelhardt M. gehen erstmals in der Veröffentlichung von 2019 bezüglich 5. GOTS-Expertenmeeting „Knorpel und Arthrose im Sport“ der Gesellschaft für Orthopädisch-Traumatologische Sportmedizin mit einem eigenen Teil auf Ernährung und Nahrungsergänzung ein. Die fehlende zyklische Ernährung wird hier mit negativen Auswirkungen auf den Stoffwechsel, mangelnder Diversifikation auf das Mikrobiom (Smits et al. 2017) und Übergewicht als systemische Entzündung erkannt. Auf eine Metaanalyse und Review von 20 Nahrungsergänzungsmitteln (Liu X. et al. 2018), die in 69 förderfähigen Studien untersucht wurden, zeigten 7 (Kollagenhydrolysat, Passionsfrucht-schalenextrakt, Curcuma longa-Extrakt, Boswellia serrata-Extrakt, Curcumin, Pycnogenol und L-Carnitin) große (Effektgröße > 0,80) und klinisch wichtige Wirkungen zur kurzfristigen Schmerzreduktion. Weitere 6 (nicht denaturiertes Typ-II-Kollagen, Avocado-Sojabohnenextrakt, Methylsulfonylmethan, Diacerein, Glucosamin und Chondroitin) zeigten statistisch signifikante Verbesserungen der Schmerzen, waren jedoch von unklarer klinischer Bedeutung. Lediglich Grünlippmuschelextrakt und nicht denaturiertes Typ-II-Kollagen hatten mittelfristig klinisch wichtige Auswirkungen auf die Schmerzen. Auf einige Stoffe wird hier im Einzelnen eingegangen.
Eiweiß & co.
Der Muskelkater ist die häufigste Nebenerscheinung bei sportlichen Aktivitäten und wird als Muskelverletzung Typ 1B oder DOMS (Delayed-Onset Muscle Soreness) klassifiziert, weil er typischerweise mit Schmerzen in den Muskeln 12–18 Stunden nach der meist exzentrischen Belastung, einem plötzlichen Anstieg der Trainingsintensität oder des Trainingsumfanges auftritt. Er ist die Folge unzähliger kleiner Schädigungen im kontraktilen Apparat der Muskulatur, die dabei auch leicht entzündet oder sogar angeschwollen ist. Durch Muskelkater kann es zu einem temporären Kraftverlust von bis zu 30 % kommen und bei falscher Folgebelastung zu schwereren Muskelverletzungen. Aktuell wurden Präventions- und Behandlungsmöglichkeiten mit Ernährungshinweisen von Hoftiel T. (2019) und Heiss R. (2018) veröffentlicht. Entzündlich wirkendende (proinflammatorische) Zytokine wie sie Verletzungen oder unzureichender Ernährung mit Mikro- und Makronährstoffen auftreten, können damit ein reduziertes anaboles Umfeld in der frühen Trainingsphase schaffen (Nemet et al. 2002). Proinflammatorische Zytokine haben sich als Hemmer der Proteinbiosynthese gezeigt (Caiozzo et al. 1996; Frost et al. 1997) und spielen daher eine negative Rolle bei der Regeneration muskulärer Belastungen. Umso mehr ist auf eine ausreichende Eiweißzufuhr zu achten. Eiweiß kann der Körper im Gegensatz zu Kohlenhydraten und Fett nicht speichern. Entweder baut er es im Rahmen von Reparatur und Regenerationsprozessen in Strukturen ein oder er verbrennt es. Daher ist die zeitliche richtig eingenommene Menge und Qualität so wichtig. Im Leistungssport werden 2 g Eiweiß pro kg / KG empfohlen. Mindestens 20–25 g hochwertiges Eiweiß (hoher Anteil essentieller Aminosäuren) führen, je früher nach jeder Belastung eingenommen, zu einer erhöhten Einbaurate und damit schnellerer Regeneration. Neuere Studien empfehlen bei Ganzkörperbelastung 40 g hochwertiges Eiweiß. So kommt es zu einem Anstieg der muskulären Proteinbiosynthese bei 20 g nach Belastung von 35 % / h gegenüber 48 % / h bei Gabe von 40 g bei jungen Männern, der aber insgesamt als geringe Steigerung zu bewerten ist (Stokes T. et al., 2018). Der Abstand solcher Proteinzufuhr von ca. 3–4 Stunden sollte nicht unterschritten werden. Ein hoher Anteil an essentiellen Aminosäuren hat zudem einen höheren Effekt (Molke Eiweiß /Whey protein) und einem hoher Leucingehalt wird eine anabole Schlüsselfunktion zugeschrieben. Pflanzliches Eiweiß weißt daher niedrigere Einbauraten auf. Bei Muskelverletzungen werden inzwischen 2–2,5 g Eiweiß pro kg / KG empfohlen. In einem aktuellen Überblick (Snijders T. et al. 2019) aller Studien zur Proteinaufnahme vor dem Schlaf ergab sich bei alten und jungen Menschen, dass aufgenommenes Protein über Nacht wirksam verdaut und absorbiert wird, wodurch die Proteinsyntheseraten über Nacht erhöht werden und damit als eine wirksame Interventionsstrategie angewendet werden kann, um die anpassungsfähige Reaktion der Skelettmuskulatur auf das Training zu unterstützen. Auch hier zeigte sich, dass ältere Menschen gegenüber jungen eine geringere Einbaurate haben (anabole Resistenz). Idealerweise sollte bei Athleten die Eiweißaufnahme über mindestens vier Mahlzeiten erfolgen. Kreatin, welches nicht nur leistungssteigernd ist, wirkt sich bei Verletzungen, Immobilität und Rehatraining positiv auf Kraft und Masseverlust aus. β-Hydroxy-β-methylbutyrat (HMB) ist ein Leucin-Metabolit, welcher die Muskelproteinsynthese beschleunigt und bei längerer Einnahme die Muskelmasse bei Bettruhe schützt. Ernährung kann jedoch nicht nur in der Regeneration, sondern auch in der Prophylaxe eingesetzt werden.
Omega-3-Fettsäuren
Die Gabe von Omega-3 Fettsäuren vor einer Belastung, die geeignet war, Muskelkater zu verursachen, konnte den initialen Anstieg der CK (Kreatinkinase) im Serum sowie den typischen Anstieg inflammatorischer Cytokine, die Schwellung des Muskels und den Kraftverlust minimieren. Omega 3 Fettsäuren sind wesentliche Bestandteile der Zellmembran. Sie bilden im Körper wichtige Strukturlipide und beeinflussen die Muskelfunktion sowie Entzündungs- und Immunreaktionen (Smith GI. 2011; McGlory C. 2014). Die anti-inflammatorischen Effekte von Eicosapentaensäure (EPA) und Docosahexaensäure (DHA) dürften für die klaren Verbesserungen von Schmerz und anderen Symptomen bei Patienten mit rheumatoider Arthritis verantwortlich sein (Senftleber NK. 2017). Arachidonsäure (Omega-6 Fettsäure) sollte z.B. bei Rheumatikern in der Ernährungsberatung deutlich reduziert werden, da sie entzündlich wirkt. Maritime Omega-3 Fettsäuren weisen eine eindeutig bessere Bilanz als pflanzliche auf. Ein neuer Ansatz erfolgt über die Zucht von EPA und DHA bildender Mikroalgen (Schizochytrium) (Nehls M. 2018). Omega-3 Fettsäuren schützen vor kardiovaskulären Risiken und unterstützen Regenerationsprozesse im Sport. Sie stimulieren über Signalproteine die muskuläre Proteinbiosynthese. Es gibt zunehmend Hinweise darauf, dass Omega-3-Fettsäuren, die aus Fischöl gewonnen werden, die Zunahme der Muskelmasse bei älteren Erwachsenen stimulieren, indem sie die durch Alterung hervorgerufene anabole Resistenz im Rahmen der Sarkopenie überwinden (Smith GI. 2011). Insbesondere DHA findet sich in hohen Konzentrationen im Gehirn und übt einen Schutzmechanismus auf zellulärer und neuronaler Ebene aus, einschließlich der Modulation von Entzündungskaskaden nach traumatischen Hirnverletzungen (Trojian TH. 2017). Hoher Fischkonsum fördert bei Kindern Intelligenz und gesunden Schlaf (Jianghong L. 2017). Das Verhältnis von Omega-6 zu Omega-3 sollte wie bei unseren Vorfahren oder den Inuit ca. 1–4:1 betragen. Daher sind Messungen als Vorrausetzungen für valide Studienergebnisse umso wichtiger. Aufgrund der schlechten Ernährung finden wir oft Verhältnisse von Arachidonsäure (Omega 6 FS) zu EPA (Omega 3 FS) von 10–20:1 auch bei Sportlern. Hier besteht ein höheres entzündliches Potenzial, höhere Verletzungsgefahr und eine schlechtere Regeneration. Eine Substitution ist daher erforderlich. 2 g Omega-3 Fettsäuren am Tag sollten zugeführt werden. Bei Verletzungen 4 g. Aus der eigenen Praxis hier Beispiele schlechter Versorgung: Rheumapatientin 1:37, Fußballbundesliga Erstligaspieler 1:17, Veganerin 1:35, KHK Patient mit Bypass 1:33, Multiple Sklerose Patientin 1:20.
Bei 106 deutschen Elite-Ausdauersportlern fand sich einen Mangel an EPA und DHA im Zusammenhang mit niedrigem Omega 3 Index (Schacky et al. 2014). Eine neue Studie (Davinelli et al. 2019) zeigte bei 257 Ausdauerläufern einen negativen Einfluss auf das Verhältnis von Arachidonsäure zu EPA auch in Abhängigkeit der zurückgelegten wöchentlichen Laufstrecke. Da eine schlechtere Versorgung nicht angenommen werden kann, ist eher davon auszugehen, dass der Körper mehr Omega- 3 Fettsäuren benötigt, da diese vermehrt entzündungshemmend verbraucht werden. Daher dürften Sportler einen erhöhten Bedarf haben.
Sekundäre Pflanzenstoffe
Neben Vitaminen sind insbesondere sekundäre Pflanzeninhaltsstoffe in den letzten Jahren zur Reduzierung von oxidativem Stress, belastungsbedingter Muskelschmerzen und Muskelermüdung in den Fokus gerückt. Hierzu gehören Polyphenole, Carotinoide, Phytoöstrogene, Glucosinolate, Sulfide, Monoterpene, Saponine, Protease-Inhibitoren, Phytosterine und Lektine. Chlorophyll und Phytinsäure lassen sich zu keiner der genannten Gruppen zuordnen, gehören aber ebenfalls zu den sekundären Pflanzenstoffen. Inzwischen wurde die Potenz der sekundären Pflanzeninhaltsstoffe in den Pflanzen auf ihre antioxidative und vor allem entzündungshemmende Wirkung untersucht. Viele dieser Substanzen sind in der Lage, die Cyclooxygenase-2 (COX-2) -Expression deutlich zu unterdrücken, welches dem anti-entzündlichem Wirkmechanismus der nicht steroidalen Antirheumatika (NSAR) wie Ibuprofen und Diclofenac entspricht. Betanin aus der roten Beete inhibierte die Aktivität um 97 %. Die antioxidative Kapazität des Rote-Bete-Saftes war weitaus größer als bei bekannten Gemüsesäften (Reddy et al. 2005). Die COX-2-Hemmwirkungen waren vergleichbar oder größer als bei mehreren phenolischen Verbindungen (Cyanidin-3-O-Glucosid, Lycopin, Chlorophyll, B-Carotin und Bixin) und entzündungshemmenden Medikamenten (Ibuprofen, Vioxx und Celebrex). Nach 10-tägiger Supplementierung (100, 70 oder 35 mg pro Tag) hatten sich die proinflammatorischen Zytokine; Tumornekrosefaktor-alpha (TNF-α) und Interleukin-6 (IL-6) gegenüber dem Ausgangswert um 8,3 % bis 35 % bzw. 22 bis 28,3 % verringert und linderten die Entzündungen und Schmerzen bei osteoarthritischen Patienten (Pietrzkowski, Z.,2010). Granatapfel-Extrakt verbesserte die Erholung der isometrischen Kraft 2–3 Tage nach einer muskelschädlichen exzentrischen Übung und milderte damit Schmerzen und Kraftverlust (Trombold JR. et al. 2011). Ebenso zeigten Blaubeeren antioxidative und entzündungshemmende Eigenschaften und eine schnellere Regeneration nach exzentrischer Muskelbelastung (McLeay Y. et al. 2012). Auch bei entzündlichen Darmerkrankungen zeigten Anthocyanine der Heidelbeere gegenüber entzündungshemmenden Medikamenten einen besseren Effekt (Sónia R. et al. 2017). Schwarzer Johannisbeer-Nektar führte zur Verringerung der Symptome von trainingsinduziertem exzentrischem Muskelschäden (EIMD) bei 16 College-Studenten (Hutchison AT. Et al. 2014). Aufgrund des sehr hohen Gehaltes von Anthocyanin rückte jedoch die Sauerkirschen in den letzten Jahren in den Mittelpunkt und ist mit der größten Anzahl an Studien positiv belegt (Wang H. et al. 1999; Clifford MN. 2000; Bondesen et al. 2004). Das Hemmpotenzial von Montmorency-Sauerkirschen für die Glykämieregulation und anderer entzündungsrelevanter Enzyme wurde von Kirakosyan A. (2018) bewertet. So wurde die α-Amylaseaktivität signifikant gehemmt, milde Hemmung der α-Glucosidase und Inhibition von Angiotensin I- 89 % (Bluthochdruck). Starke bis mäßige Hemmungen von Cyclooxygenase-1 (65%), Lipoxygenase (64%), Cyclooxygenase-2 (38%) bzw. Xanthinoxidase (Harnsäuresenkung), (26%). Anthocyane, Cyanidin-3-Rutinosid und Cyanidin-3-Glucosid waren starke Inhibitoren von α-Amylase und α-Glucosidase. Kirakosyan A. (2018) kommt zum Schluss, dass die Hemmung all dieser Enzyme eine starke biochemische Grundlage für das Management von Typ-2-Diabetes und Herz-Kreislauf-Erkrankungen bietet, indem die Glukoseabsorption gesteuert und die damit verbundene Hypertonie und Entzündung reduziert werden. Im aktuellen Review für Montmorency-Sauerkirschen (Kelley DS. et al. 2018) dauerten die meisten Studien weniger als 2 Wochen (5h bis 3 Monate) und wurden mit einem Äquivalent von 45 bis 270 Kirschen / Tag (Anthocyane 55–720 mg / Tag) in Einzel- oder aufgeteilten Dosen durchgeführt. Die Einnahme verbesserte die Leistung, Erholung, Muskelkater und entzündliche Serumparameter bei 16 gesunden Fußballern (Bell 2016). Bei 27 Läufern und Triathleten verbesserte sich die Marathonzeit, senkten sich die Marker für Muskelkatabolismus, oxidativen Stress und Entzündung im Vergleich zu Placebo bei einer Einnahme 10 Tage vor bis 2 Tage nach dem Rennen (Levers 2016). Bei 20 Marathon Läufer(innen) senkten sich nach dem Rennen Entzündungsparameter und Schmerz bei Einnahme 5 Tage vor und 2 Tage nach dem Rennen (Howatson 2010). Nach dem Training bei Radfahrern, die Kirschsaft 7 Tage zuführten, war die Interleukin-6-Konzentration um 200 % niedriger (Bell 2014). Bei 10 gesunden Frauen, die an einem Tag 280 g Kirschen zuführten, waren die Entzündungswerte niedriger und die Harnsäurespiegel gesunken (Jacob RA. et al. 2003). Durch die Einnahme von Kirschen konnte in einer 7-jährigen Studie der Boston University School of Medicine bei 633 Gicht-Patienten das Risiko für Gichtanfälle um 35 % gesenkt werden (Yuqing Zhang et al. 2013). Gicht tritt als Folge der Kristallisation von Harnsäure in Gelenken auf und verursacht Schwellung und Schmerzen in den damit verbundenen Bereichen. Ziel im Leistungssport ist eine Harnsäure < 5 mg / dl um Muskeln und Sehnen zu schützen. Im Rückblick (Kelley DS. et al. 2018) auf alle evidenten Studien verringerte der Verzehr von Kirschen die Marker für oxidativen Stress in 8 von 10 ; Entzündung in 11 von 16; belastungsinduzierten Muskelkater (DOMS) und Kraftverlust in 8 von 9; senkte den Blutdruck in 5 von 7 und eine Arthritis in 5 von 5 Studien.
Der Schlaf verbesserte sich wohl auch aufgrund des Melatoningehaltes in 4 von 4 Studien. Kirschen reduzierten auch das Hämoglobin A1C (HbA1C), das Lipoprotein sehr niedriger Dichte (VLDL) und Triglyceride / High-Density-Lipoprotein (TG / HDL) bei diabetischen Frauen und VLDL und TG / HDL bei übergewichtigen Teilnehmern.
Neue Ergebnisse deuten darauf hin, dass eine einmalige Supplementierung mit 30 ml Montmorency Sauerkirschsaft 1,5 h vor Belastung bei trainierten Radfahrern den Blutdruck senkt und einige Aspekte der Trainingsleistung, insbesondere der Endsprint-Leistung, verbessern kann (Keane KM. et al. 2018).
Gewürze
Nicht nur Früchte und Beeren, sondern auch Gewürze haben entzündungshemmende Eigenschaften. So wurde das vielversprechende Kurkumin aus der Gelbwurz inzwischen sehr gut untersucht. Es wurde gezeigt, dass Kurumin antioxidative, entzündungshemmende, anti-carcinoge, anti-angiogenese, chemopräventive und chemotherapeutische Eigenschaften besitzt (Akram et al. 2010; Li et al. 2011). Es erwies sich als wirksam zur Schmerzlinderung bei arthritischen Patienten (Li et al. 2011). Eine Verbesserung der Sehnenheilung und -funktion beruhte auf ihren antioxidativen und entzündungshemmenden Eigenschaften, die mit gut organisierten Kollagenfasern und einer extensiven Kollagenablagerung im regenerierten Sehnengewebe in Verbindung stehen (Jiang D.et al. 2016). Weihrauch (Bowswellia Extract / BSE) besitzt immunmodulatorische Eigenschaften und verändert das Zytokinproduktionsprofil positiv (Ammon H.P.T. 2010). Boswelliasäuren im Weihrauch hemmen die Leukotrienbiosynthese und wirken somit entzündungshemmend, ohne die Nebenwirkungen, wie sie von NSAR bekannt sind. Weihrauch beschleunigte auch die Funktionswiederherstellung und verminderte Schmerzen sowie objektive körperliche und humorale Anzeichen von Entzündungen bei Personen mit Arthritis (Belcaro G. 2015). Boswellia serrata hat auch die Fähigkeit gezeigt, entzündungsfördernde Zytokine zu hemmen. Es unterdrückt Interleukin-1β (IL-1β), Tumornekrosefaktor-α (TNF-α), Interferon-γ (IFN-γ) und erhöht die Produktion von IL-10 bei Ratten mit Kollagen-induzierter Arthritis. Diese Zytokine spielen eine entscheidende Rolle bei chronischen Entzündungen und Gewebeschäden während des Fortschreitens der rheumatoiden Arthritis (Zhang JM. 2007; Singh D. 2013). Kumar R. (2019) belegen die Bedeutung von BSE als potenzielles Mittel gegen Arthritis und empfehlen die Kombination von BSE als Ergänzung zur konventionellen modernen Therapie bei der Behandlung von RA. Eine Kombination aus Kurkumin und Weihrauch war erwiesenermaßen sicher und effizient bei Patienten mit Arthrose, objektive Symptome zu lindern. Die Kombination zeigte sich besser als Celecoxib (Celebrex = ein selektiver COX-2-Inhibitor) und war zusätzlich zu den entzündungshemmenden Eigenschaften praktisch ohne Nebenwirkungen.
12-wöchiger Gebrauch von Kurkumin-Komplex oder seine Kombination mit Weihrauch reduziert schmerzbedingte Symptome bei Patienten mit Osteoarthritis (Haroyan A. 2018). Kurkumin war in Kombination mit Weihrauch effektiver und erhöhte die Wirksamkeit der Behandlung von Osteoarthritis. Kurkumin übt polyvalente pharmakologische Wirkungen und Multi-Target-Effekte aus, einschließlich Schmerzlinderung und anti-nozizeptive Aktivität. Seo EJ. et (2018) berichten zum ersten Mal, dass Kurkumin und Weihrauch als Antagonisten von Nociceptin-Rezeptoren fungieren, indem sie selectiv das opioid-bezogene Nociceptin-Rezeptor 1-Gen herunterregulieren (OPRL1), was mit einer Schmerzlinderung verbunden ist.
Enzyme
Enzyme werden standardisiert bei Muskelverletzungen zur Regeneration gegeben werden. Sie wirken über eine Regulation Zytokinspiegel, Einfluss auf Blutrheologie (Plättchenaggregation, Fibrinolyse), Ödemreduktion (Abschwellung) und die Reduktion von Immunkomplexen. Aber auch präventiv zeigen sie positive Effekte. Marzin et al. (2017 ) zeigte in einer Placebo-kontrollierten Doppelblindstudie an 72 Sportlern beispielsweise, wie eine Enzymkombination mit Bromelain, Trypsin und Rutosid die Regeneration nach Belastungen fördert und potenzielle Muskelschädigungen bei Ausdauersportlern abmildert. Bei allen untersuchten Sportlern konnte ein Einfluss auf Biomarker des Muskelstoffwechsels, der Entzündung und des Immunstatus gezeigt werden.
Nicht-denaturiertes Typ-II-Kollagen
Neuere Studien zeigen auch gute entzündungshemmende Eigenschaften von nicht denaturiertem Typ-II-Kollagen auf und wie dies Tiere bei experimentell induzierter Arthritis vor Gelenkschäden schützt (Asnagli H. et al. 2014). Es wird angenommen, dass dieser Schutz über die Induktion und Migration von T-regulatorischen Zellen (Tregs) in den Bereich der Entzündung und Schädigung erfolgt (Weiner HL. Et al., 2011). Die vorgeschlagene Rolle von T-regulatorischen Zellen könnte auch für die Milderung von osteoarthritischen (OA) -Symptomen relevant sein, da In-vitro-Studien gezeigt haben, dass Tregs entzündungshemmende Zytokine produzieren, die Chondrozyten zur Synthese von Knorpelmatrixkomponenten anregen (van Meegeren ME., EJ. 2012). Eine aktuelle randomisierte, placebokontrollierte doppelblind Studie mit 164 Patienten ergab, dass sich mit 40 mg nicht denaturiertem Typ-II-Kollagen (UC-II®), die Kniefunktion bei OA-Patienten bis zum Tag 60 im Vergleich zu Placebo und bis zum Tag 180 auch gegenüber Glucosamin und Chondroitinsulfat (1500 mg G, 1200 mg C), signifikant verbesserte und gut vertragen wurde (Lugo JP. et al. 2016). Jüngste präklinische Studienergebnisse belegen, dass eine klinisch relevante Tagesdosis von UC-II® unmittelbar nach Verletzung die mechanische Funktion des betroffenen Knies verbessern und eine übermäßige Verschlechterung des Gelenkknorpels verhindern kann (Bagi C.M. et al. 2017).
Autoren
» Facharzt für Allgemeinmedizin und Arbeitsmedizin mit Zusatzbezeichnungen u. a. Chirotherapie und Sportmedizin
» Leitender Arzt BG Prevent GmbH, Darmstadt
» 2011–2020 Teamarzt SV Darmstadt 98 (2015–2022 im NLZ), 2022–2023
Ergänzung med. Team des 1. FC Kaiserslautern (Ernährungsmedizin, Regeneration- und Leistungsmedizin & Mannschaftsarzt), 2002–2014 med. Leiter Ironman Germany
(Stand 2026)
(Stand 2026)
ist Verbandsarzt der Deutschen Triathlon Union (DTU). Neben der klinischen Tätigkeit im Zentrum für Muskuloskelettale Chirurgie (OZMC) des Klinikums Osnabrück beschäftigt er sich wissenschaftlich schwerpunktmäßig mit Muskel- und Sehnenverletzungen und kann auf diesem Gebiet eine Vielzahl internationaler Publikationen vorweisen. Er ist Vorstandsmitglied der GOTS, Mitglied des GOTS-Komitees Muskel, Mitglied im „Muscle Research Center Erlangen“ (MURCE) und wiss. Beirat der sportärztezeitung.



