Peptide stellen eine zentrale Klasse biologisch aktiver Moleküle dar, die regulatorische Funktionen in nahezu allen Organsystemen ausüben [1, 2]. Besonderes Interesse gilt ultrakurzen Peptiden (Ultrashort Peptides, USPs) mit 2 – 7 Aminosäuren, da sie eine ausgeprägte Gewebe- und Funktionsspezifität besitzen und direkt in die Regulation der Genexpression eingreifen können [1 – 3]. Ziel dieser Übersichtsarbeit ist es, vier thematische Schwerpunkte zusammenzuführen: (1) USPs als Bioregulatoren in Orthopädie und Sportmedizin, (2) peptidvermittelte Regulation der Genexpression, (3) neurogene Differenzierung durch AEDG (Epitalon) und (4) peptidbasierte Steuerung der chondrogenen Stammzelldifferenzierung.
(1) Ultrakurze Peptide in Orthopädie und Sportmedizin
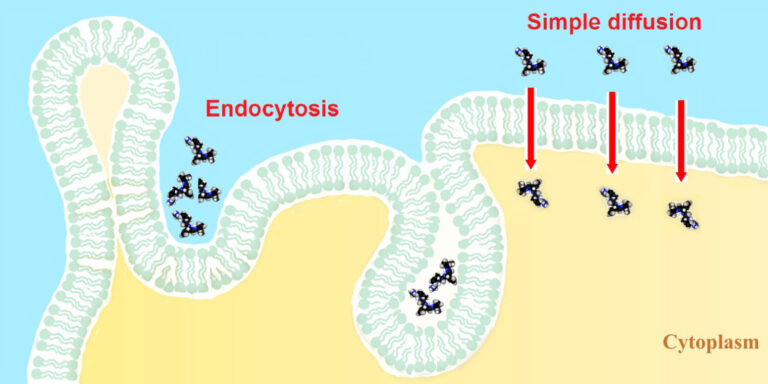
Ultrakurzpeptide bestehen aus 2 – 7 Aminosäuren und besitzen aufgrund ihrer geringen Größe (≈1,3 – 1,8 nm) besondere pharmakokinetische Eigenschaften [1, 3, 4]. Im Vergleich dazu weist eine klassische α-Helix eine Länge von etwa 2,1 nm auf. Diese Größenrelation ermöglicht es USPs, Zellmembranen, das Zytoplasma und den Zellkern ohne klassische Rezeptorbindung zu überwinden (Abb. 1) [3 – 5]. Damit unterscheiden sie sich grundlegend von Peptidhormonen oder Wachstumsfaktoren, deren Wirkung überwiegend membranrezeptorvermittelt ist. In der Orthopädie und Sportmedizin werden USPs mit verbesserten regenerativen Prozessen in Muskel-, Sehnen- und Knorpelgewebe in Verbindung gebracht [6 – 8]. Experimentelle Arbeiten zeigen eine Modulation der Expression von Strukturproteinen (z. B. Kollagene), Enzymen des Energiestoffwechsels sowie entzündungsregulatorischen Zytokinen [2, 6]. Klinisch werden Effekte wie beschleunigte Regeneration nach Belastung, verbesserte Trainingsadaptation, Reduktion muskuloskelettaler Überlastungssyndrome und eine stabilisierte Immunfunktion beschrieben [6 – 8]. Besonders relevant ist die Beobachtung, dass USPs nicht primär leistungssteigernd im Sinne klassischer Dopingmechanismen wirken, sondern die physiologische Anpassungsfähigkeit erhöhen [7, 8]. Dies umfasst eine verbesserte Stressresilienz, eine ökonomischere muskuläre Koordination sowie eine reduzierte Infektanfälligkeit in intensiven Trainingsphasen. Aufgrund ihrer guten Verträglichkeit und der fehlenden Aufnahme in die WADA-Dopingliste besitzen USPs eine Sonderstellung im Leistungssport.
(2) Peptidregulation der Genexpression
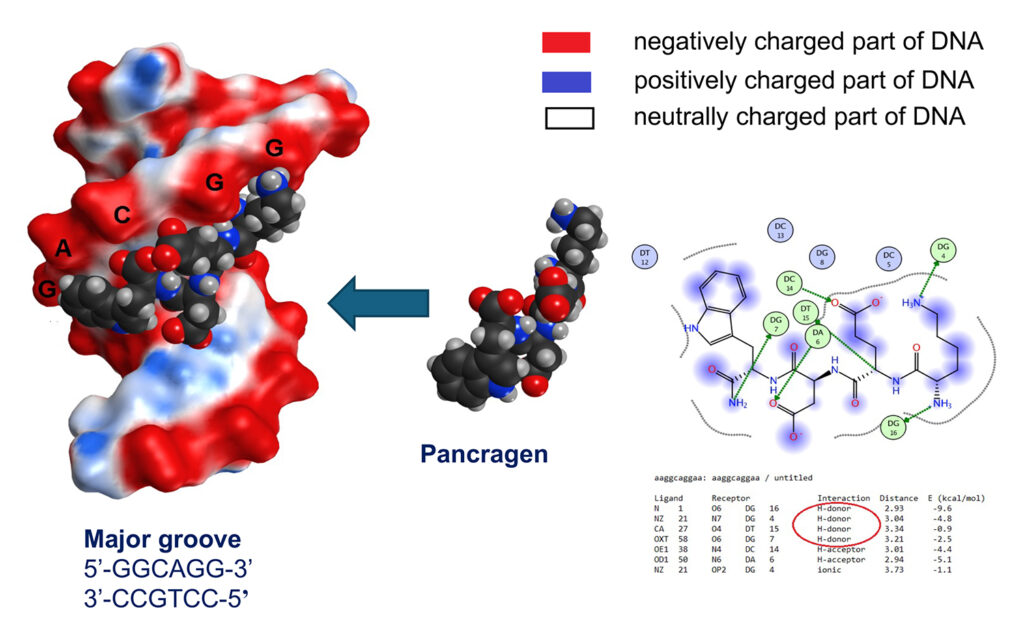
Die Fähigkeit kurzer Peptide, direkt mit dem Genom zu interagieren, stellt einen Paradigmenwechsel in der molekularen Regulation dar [2, 3, 9]. In-vitro und in-silico-Studien zeigen, dass Peptide mit definierter Aminosäuresequenz spezifische DNAMotivikationen erkennen können, insbesondere in Promotor und Enhancerregionen [2, 3]. Zusätzlich zeigen sie eine hohe Affinität zu Histonproteinen, vor allem zu linker Histon-H1 sowie zu H3- und H4-Varianten [2, 9]. Diese Interaktionen führen zu konformationsabhängigen Veränderungen des Chromatins, die entweder eine Aktivierung oder Repression der Transkription bewirken [2, 9, 10]. Beschrieben wurden Effekte auf DNA-Methylierungsmuster, Histonacetylierung und die Zugänglichkeit von Transkriptionsfaktoren [2, 9]. Bemerkenswert ist, dass diese Effekte dosisabhängig auftreten und keine unspezifische globale Transkriptionsaktivierung verursachen, sondern selektiv funktionelle Gencluster beeinflussen. Evolutionär betrachtet sind peptidvermittelte Regulationsmechanismen hoch konserviert. Analoge Effekte wurden in Pflanzen, Hefen, Insekten, Nagetieren und humanen Zelllinien nachgewiesen (Abb. 2) [3, 11]. Dies unterstützt die Hypothese, dass kurze Peptide eine ursprünglichere, grundlegende Regulationsebene darstellen, die älter ist als viele hormonelle Signalwege.

(3) AEDG (Epitalon) und neurogene Differenzierung
Das Tetrapeptid AEDG (Ala-Glu-AspGly), auch als Epitalon bekannt, zählt zu den am intensivsten untersuchten Bioregulatorpeptiden [12 – 14]. Ursprünglich aus der Epiphyse isoliert, wurde AEDG mit einer Verlängerung der Lebensspanne, einer Normalisierung zirkadianer Rhythmen und einer Reaktivierung altersabhängiger Zellfunktionen in Verbindung gebracht [12, 13]. Auf zellulärer Ebene zeigt AEDG eine ausgeprägte Wirkung auf humane mesenchymale Stammzellen. Mehrere Studien belegen eine verstärkte neuronale Differenzierung, charakterisiert durch die Hochregulation neurogener Marker wie Nestin, Growth associated Protein (GAP) – P-43, β-Tubulin III, Doublecortin und MAP2 [14, 15]. Parallel dazu wird eine Suppression proliferationsassoziierter Gene beobachtet, was auf eine gezielte Förderung der Reifung neuronaler Phänotypen hindeutet. Molekulardynamische Simulationen und biochemische Analysen zeigen, dass AEDG bevorzugt an Histon-H1 sowie an H3- und H4-Domänen bindet [14, 16]. Diese Bindung führt zu einer Lockerung der Chromatinstruktur in neurogenen Genloci. Zusätzlich wurden Effekte auf die Telomeraseaktivität, oxi-
dativen Stress und die Stabilisierung von Telomerregionen beschrieben, was die Einordnung von AEDG als geroprotektives Peptid unterstützt [12, 13, 16].
(4) Peptidregulation der chondrogenen Stammzelldifferenzierung
Die Degeneration von Gelenkknorpel stellt eine der größten therapeutischen Herausforderungen der Orthopädie dar. Mesenchymale Stammzellen (englisch: mesenchymal stem cells, MSCs) bieten ein hohes regeneratives Potenzial, dessen gezielte chondrogene Differenzierung jedoch komplex reguliert ist [17]. Neben klassischen Wachstumsfaktoren wie Transforming Growth Factor beta (TGFβ) und Bone Morphogenetic Proteins (BMPs) rücken kurze Peptide zunehmend in den Fokus, da sie spezifische Signalwege modulieren, ohne die mit Wachstumsfaktoren assoziierten Nebenwirkungen [18, 19]. Peptidsequenzen, die von Knorpel-ECM-Proteinen oder Wachstumsfaktoren abgeleitet sind (z. B. Arginin-Glycin-Aspartat (RGD-), Collagen-Phenylalanin-Glycin-Glutamat-Arginin (CFOGER-), N-Cadherin- oder Bone-Morphogenetic-Protein-mimetische (BMP-mimetische Peptide), aktivieren gezielt Smad-, Wnt/β-Catenin- (WNT-) und Mitogen-activated-protein-kinase (MAPK-) Signalwege [18 – 20]. Dies führt zu einer gesteigerten Expression zentraler chondrogener Marker wie Sex-determining-region-Y-box-9- (SOX9-) und Kollagen-Typ-IIAlpha-1 (COL2A1-) und Aggrecan sowie zu einer verbesserten extrazellulären Matrixorganisation [18 – 20]. Im Vergleich zu rekombinanten Wachstumsfaktoren zeichnen sich Peptide durch eine höhere Stabilität, bessere Steuerbarkeit der Dosis-Wirkungs-Beziehung und ein geringeres Risiko ektoper Ossifikation aus [17, 19]. Diese Eigenschaften machen sie zu vielversprechenden Kandidaten für zukünftige zellbasierte Therapiestrategien bei Osteoarthritis und posttraumatischen oder degenerativen Knorpelschäden.
Diskussion und Schlussfolgerung
Über alle vier Themengebiete hinweg zeigt sich ein konsistentes Wirkprinzip ultrakurzer Peptide: Sie wirken primär über epigenetische Mechanismen auf Ebene der Genexpression (Abb. 3) [2, 3, 9]. Ihre hohe Spezifität, geringe Toxizität und orale Bioverfügbarkeit machen sie zu attraktiven Kandidaten für regenerative Medizin, Sportmedizin, Neuroregeneration und Arthrosetherapie [6 – 8,12 –15]. Die Evidenzlage ist jedoch heterogen. Während für bestimmte Peptide (z. B. AEDG / Epitalon, KE, KED, AEDL) umfangreiche präklinische Daten sowie kleinere klinische Studien vorliegen, fehlen für viele Anwendungen randomisierte, placebokontrollierte Multicenterstudien nach westlichen Evidenzstandards [2, 12]. Zukünftige Forschung sollte sich auf standardisierte klinische Studien, Dosis-Wirkungs-Beziehungen und kombinierte Therapieansätze konzentrieren.
Literatur
- Morozov VG, Khavinson VK. Natural Peptide Bioregulators. St. Petersburg: Nauka; 1983.
- Khavinson VK, Popovich IG, Linkova NS, et al. Peptide regulation of gene expression: a systematic review. Molecules. 2021;26:7053.
- Khavinson VK, Anisimov SV, Malinin VV, Anisimov VN. Peptide Regulation of the Genome and Aging. Moscow: RAMS; 2005.
- Anisimov VN, Khavinson VK. Peptides and aging. Neuroendocrinol Lett. 2010;31(Suppl 1):1–7.
- Ilina AR, Linkova NS, Khavinson VK. Neuroepigenetic effects of ultrashort peptides. Int J Mol Sci. 2022;23:4259.
- Taimazov VA, Tsygan VN, Mokeeva EG. Sport and Immunity. St. Petersburg: Olymp SPb; 2003.
- Taimazov SA, Bakulev SE. Predicting athletic performance considering genetic trainability. Sci Notes Lesgaft Univ. 2005;18:81–91.
- Khavinson VK, Linkova NS. Peptide regulation of adaptation processes in athletes. Bull Exp Biol Med. 2018;165:1–6.
- Khavinson VK, Linkova NS, Diatlova A, et al. Peptide regulation of cell differentiation. Stem Cell Rev Rep. 2020;16:118–125.
- Kouzarides T. Chromatin modifications and their function. Cell. 2007;128:693–705.
- Maestri E, Marmiroli M, Marmiroli N. Bioactive peptides in plant‑derived food. Trends Food Sci Technol. 2016;50:134–144.
- Anisimov VN, Khavinson VK. Epitalon and longevity. Biogerontology. 2012;13:421–432.
- Khavinson VK, Bondarev IE. Telomere elongation under influence of short peptides. Bull Exp Biol Med. 2014;157:511–514.
- Khavinson VK, Diomede F, Mironova E, et al. AEDG peptide stimulates gene expression during neurogenesis. Molecules. 2020;25:609.
- Diomede F, et al. Short peptides and neural differentiation of MSCs. Int J Mol Sci. 2021;22:10344.
- Ilina AR, Khavinson VK. Epigenetic mechanisms of AEDG peptide. Neurochem J. 2021;15:219–226.
- Bernardo ME, et al. Mesenchymal stromal cells: mechanisms of differentiation and clinical applications. Bone. 2007;40:703–714.
- Linkova NS, Khavinson VK, Diatlova A, et al. Peptide regulation of chondrogenic stem cell differentiation. Int J Mol Sci. 2023;24:8415.
- Ustun Yaylaci S, et al. Chondrogenic differentiation on GAG‑mimetic peptide nanofibers. ACS Biomater Sci Eng. 2016;2:871–878.
- Szychowski KA, Skóra B. Elastin‑derived peptides affect gene expression in hMSCs. Cytokine. 2024;172:156146.
An dem Artikel hat als Co-Autor Werner Ulrich (The Bioregulator Company) mitgearbeitet.
Autoren
» Facharzt für Innere Medizin mit Fort- und Weiterbildung als Ernährungsbeauftragter Arzt (DAEM/DGEM)
» SP Gastroenterologie, Endokrinologie, diabetologie, komplementäre und gastroenterologische Onkologie
» Swiss Medical Clinic AG, Adliswil/Zürich, Schweiz + Integrative Cancer Care
(Stand 2026)