Der plötzliche Herzstillstand (sudden cardiac arrest; SCA) ist die häufigste Ursache für den plötzlichen Herztod (PHT) bei Sportlern. PHT ist definiert als ein unerwarteter natürlicher Tod aufgrund kardialer Ursachen, der innerhalb von einer Stunde nach Einsetzen der Symptome bei einer Person mit bekannter oder unbekannter Herzerkrankung auftritt [1].
Während bei Sportlern > 35 Jahre die koronare Herzkrankheit (KHK) führende Ursache des PHT ist, wird bei Sportlern unter < 35 Jahre eine arrhythmogene Ursache bei häufig zugrunde liegender struktureller oder elektrischer Herzpathologie beobachtet [1 – 4]. In dem Zusammenhang ist die hypertrophe- oder Compaction-Kardiomyopathie, gefolgt von Koronaranomalien (atypisch aus dem rechten (vorderen) Sinus Valsalva abgehende linke Koronararterie), bzw. eine akute Aortendissektion neben hereditären Ionenkanalerkrankungen (u. a. Brugada-Syndrom) die Hauptursache für den PHT [4].
Plötzlicher Herztod (PHT) bei Sportlern – Unklare Inzidenz
Die genaue Häufigkeit des PHT bei Sportlern ist aufgrund des Fehlens einer Meldepflicht und bisher nicht strukturierter Methoden zur Untersuchung der Inzidenz, nicht exakt bekannt. Aktuelle Schätzungen der jährlichen Inzidenz des plötzlichen Herztodes bei Sportlern reichen von fast einem von 1 : 1.000.000 [5] bis zu 1 : 23.000 [6] Sportlern, während für besonders gefährdete Subpopulationen von Sportlern deutlich höhere Inzidenzen von bis zu 1:3.000 dokumentiert wurden [7]. Obwohl zuletzt publizierte Daten das z. T. auch wieder anzweifelten, wird in den meisten Publikationen eine PHT-Inzidenz von ca. 1:200.000 angenommen [8 – 10]. Bezüglich des Auslösens einer arrhythmogenen Ursache eines PHT durch sportliche Aktivität (bei Sportlern mit kardialer Vorerkrankung) bestehen aber insgesamt keine Zweifel.
Risikostratifizierung: Wer ist gefährdet?
Das EKG ist das zentrale und entscheidende diagnostische Screening-tool zur Erkennung von strukturellen- (u. a. hypertrophe Kardiomyopathie (HCM), arrhythmogene rechtsventrikuläre Dysplasie/Ventrikel) sowie Leitungsanomalien wie Long-QT- oder WPW-Syndromen. Die zweidimensionale transthorakale Echokardiographie ist das wichtigste diagnostische Instrument zur klinischen Erkennung vieler kardialer Pathologien, insbesondere zur Diagnose und Nachsorge der HCM, und kann darüber hinaus auch andere relevante Auffälligkeiten erkennen, die möglicherweise für eine PHT bei jungen Sportlern verantwortlich sind. Hierzu gehören linksventrikuläre Kontraktionsauffälligkeiten, z. B. aufgrund einer Myokarditis oder dilatativer Kardiomyopathie, Herzklappenerkrankung und Aortenwurzelerweiterung. Eine erbliche oder sportbedingte arrhythmogene rechtsventrikuläre Kardiomyopathie ist allein durch die Echokardiographie oft schwer zu diagnostizieren, weshalb hier in der Regel ein kardiales MRT in Erwägung gezogen wird. Angeborene Koronaranomalien können ebenfalls nur mittels CT-Angiographie, MRT oder invasiv mittels Koronararteriographie diagnostiziert werden.
Arrhythmierisiko für Sportler… durch Sport?
Während körperliche Aktivität wegen der Vorteile für die kardiovaskuläre Gesundheit und Prognose jedem dringlich zu empfehlen ist, ist das Risiko eines plötzlichen Herztodes während körperlicher Anstrengung unzweifelhaft erhöht. Da die Mehrheit der Herz-Kreislauf-Erkrankungen bei Sportlern während des Trainings oder Wettkampfes auftritt, müssen Sportler mit hohem Risiko für Herz-Kreislauf-Erkrankungen mit zugrunde liegenden strukturellen oder elektrischen Herzerkrankungen oft von sportlichen Aktivitäten, Training und Wettkampf ausgeschlossen werden. Obwohl automatisierte externe Defibrillatoren (AED) die Möglichkeit der sofortigen Defibrillation im Fitnessstudio bzw. während des Trainings und Wettkampfes bieten, decken sie nicht das Risiko von Herzrhythmusstörungen bei starken Belastungen im normalen Leben und außerhalb des Fitnessstudios ab.
Indikationen für Intracardiale Defibrillatoren (ICD)
Implantierbare Intracardiale Defibrillatoren (ICD) sind die anerkannte lebensrettende Therapieoption für Personen mit arrhythmogenem PHT-Risiko sowohl bei der Primär- [11] als auch bei der Sekundärprävention [12] von arrhythmogenen Ereignissen. Während die erste ICD-Generation nur zur Defibrillation in der Lage war, bietet die aktuelle ICD-Technologie mittels transvenös implantierter Sonde im rechten Ventrikel (TV-ICD), eine adäquate Erkennung von ventrikulären Arrhythmien sowie Therapiemöglichkeiten bei bradykarden oder tachykarden Rhythmusstörungen mittels antibradykarder bzw. antitachykardie-Stimulation (ATP).
Transvenös-implantierte ICD (TV-ICD) – bewährte Technologie aber…
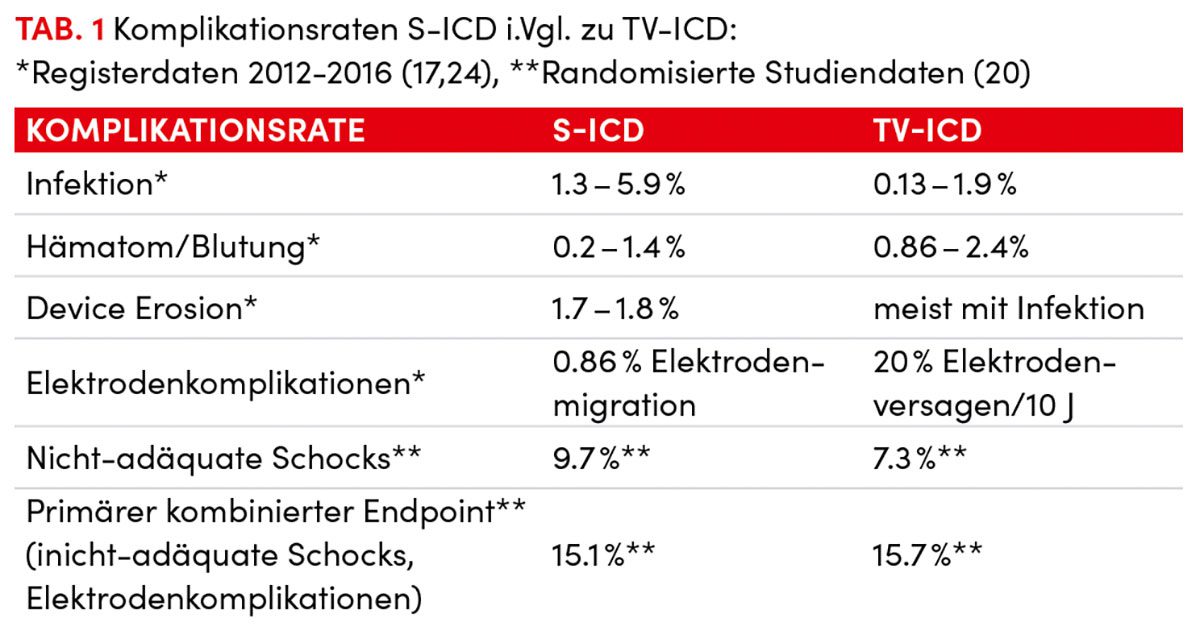
Trotz jahrelanger positiver Erfahrungen und nachgewiesener Wirksamkeit beinhaltet die TV-ICD Technologie jedoch auch potenzielle Komplikationen, wie lokalisierte Taschen-, Wund- oder systemische Infektionen, Komplikationen im Zusammenhang mit dem Gefäßzugang (u.a. Pneumothorax, Venenthrombose) Elektrodendislokation bzw. Elektrodenfehlfunktionen durch Perforation, die häufig bewegungsassoziiert sind (Sportler). Die Implantation transvenöser Elektroden ist bei Kindern aufgrund der kleineren Venenkaliber und des voranschreitenden Wachstums bzw. bei Patienten mit venösen Anomalien oder anatomisch kleinem Thorax-outlet (häufig bei Kraftsportlern), problematisch. Darüber hinaus sind ICD-Elektroden nicht selten die Ursache für eine hämodynamisch relevante Trikuspidalinsuffizienz und das Risiko einer Elektrodenfraktur ist bei körperlich aktiven Patienten (Sportler) signifikant häufiger [13]. Die dann notwendige Elektrodenextraktion geht mit einem nicht zu unterschätzendem Morbiditäts- und Mortalitätrisiko einher [14] (Tab 1).
…die bessere ICD-Alternative bei Sportlern: S-ICD
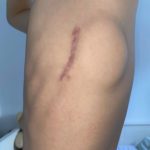
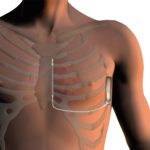
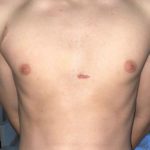
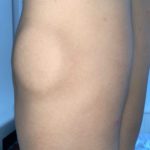
Angesichts der meist von den transvenös eingebrachten Elektroden ausgehenden Komplikationen bzw. Einschränkungen des Nutzen-Risikos der TV-ICD Systeme, wurde das vollständig mitsamt Elektroden subkutan zu implantierende subkutane ICD-System (S-ICD) entwickelt und seit 2009 in Europa zugelassen, um den lebensrettenden Nutzen des konventionellen TV-ICD zur Prävention lebensbedrohender Arrhythmien ohne den von den transvenös implantierten Elektroden ausgehenden Unzulänglichkeiten von TV-Elektoden-ICD-Systemen zu haben. S-ICDs bestehen aus einem Aggregat (80 J inklusive biphasischem Schocksystem) in einem Titangehäuse, das im linken Thoraxbereich implantiert wird, wobei die Gerätetasche im 5. Interkostalraum zwischen der mittleren und vorderen Axillarlinie liegt (Abb. 1) und die subkutan implantierte Elektrode ca. 1 – 2 cm links von der Sternum-Mittellinie (Abb. 2 + 3) positioniert ist. Um eine ausreichende Funktion eines S-ICD-Systems zu gewährleisten, ist ein EKG-Screening zwingend erforderlich, um geeignete subkutane Wahrnehmungssignale sicherzustellen, die Sensitivität und Spezifität für die Rhythmuserkennung und -therapie zu erhöhen und das Risiko unangemessener Schocks zu reduzieren. Nur in 7 – 11 % der Fälle kann aufgrund nicht ausreichender Signale im EKG-Screening und dem dadurch erhöhten Risiko von Under- bzw. Oversensing eine S-ICD-Implantation nicht empfohlen werden [15].
S-ICD: Vergleichbar wirksam aber deutlich weniger Elektrodenprobleme
Nach mehreren Hardware- und Software Modifikationen sind die derzeit verfügbaren S-ICD-Systeme zur Erkennung und Behandlung lebensbedrohlicher ventrikulärer Arrhythmien genauso effektiv und sicher wie TV-ICDs [12, 13, 17]. Obwohl der mittlere Defibrillationsschwellentest (DFT), der zur Vorhersage der Schockwirksamkeit bei ventrikulärer Arrhythmie verwendet wird und sich auf die minimale Schockstärke bezieht bzw. das Herz adäquat defibrilliert, beim S-ICD höher ist, zeigte der subkutane ICD eine vergleichbare spontane Terminierung ventrikulärer Arrhythmien mit einem Schock in 90,1 % und innerhalb von fünf Schocks in 98,2 % der Fälle (Tab. 1) [16]. Nachdem die klinische Wirksamkeit der S-ICDs in mehreren Beobachtungsstudien nachgewiesen wurde [17, 18], unterstrichen die Ergebnisse erster randomisierter Vergleiche von S-ICD mit TV-ICDs [19], dass S-ICD-Systeme der aktuellen Generation eine valide Alternative zum TV-ICD bei Patienten mit einer ICD-Indikation und bei denen keine anti-bradykarde bzw. antitachykarde oder kardiale Resynchronisationstherapie erforderlich ist (Tab. 1) [20].
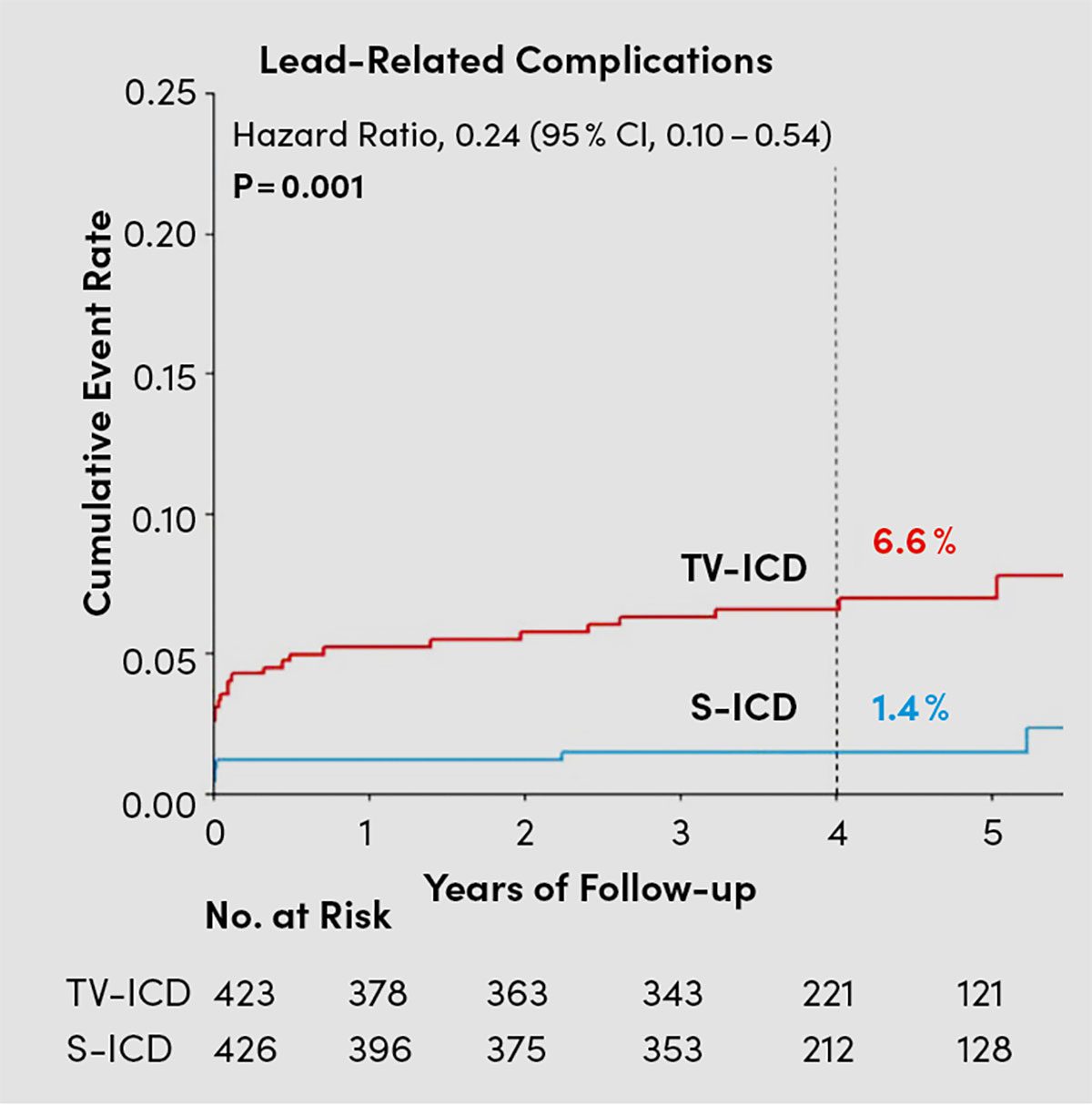
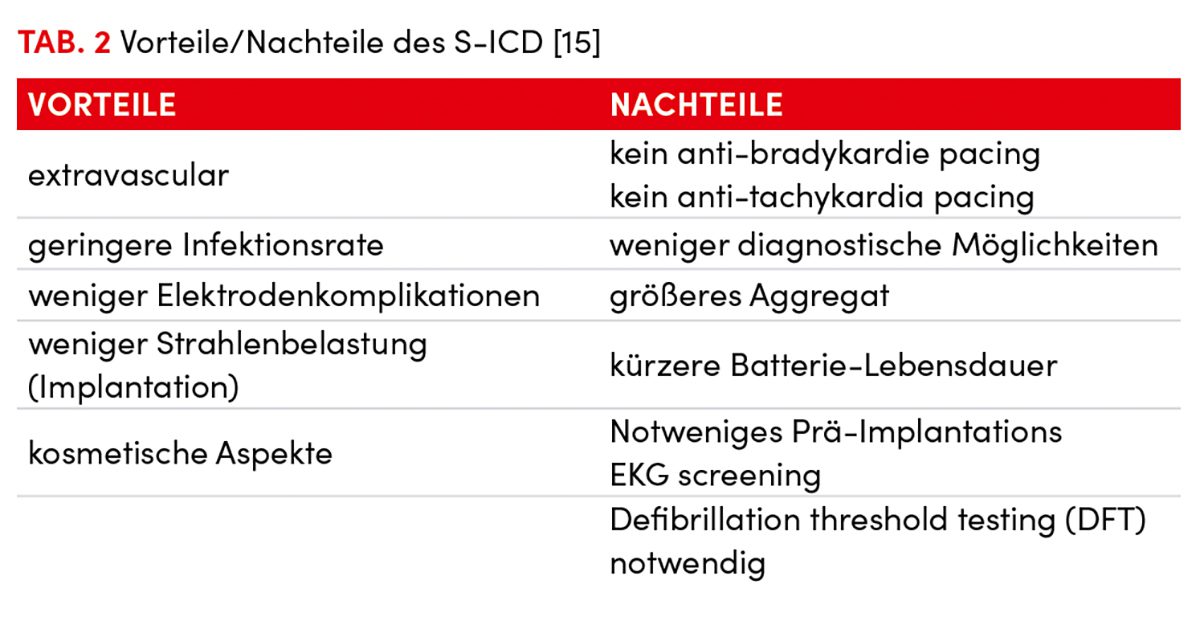
Die Elektrodenmigration mit der Notwendigkeit einer Elektrodenrevision als Hauptgrund für unangemessene Schocks konnte durch das Anlegen der Nahtmanschette, die die Elektrode an der unteren Sternuminzision sichert, effektiv auf 0,85 % reduziert werden (Abb. 3) [18, 21]. Im Vergleich zu herkömmlichen TV-Elektroden sind S-ICD-Elektroden aufgrund ihrer subkutanen Lage weniger Umweltfaktoren bzw. Bewegungen ausgesetzt [22], was insbesondere bei körperlich aktiven Patienten bzw. Sportlern der Fall ist (Tab. 2). In randomisierten Studien zeigten S-ICD daher deutlich weniger Elektrodenkomplikationen im Vergleich zu TV-ICD (Abb. 6; Tab. 1). Unangemessene Schocks konnten aufgrund der Zwei-Zonen-Programmierung, sorgfältigem EKG-Screening und verbesserter Bedienererfahrung deutlich bzw. auf die von TV-ICD [17] reduziert werden [24] (Tab. 1). Da Elektrodenkomplikationen mit der körperlichen Aktivität insbesondere Schulter-Oberarmbewegungen assoziiert sind, sind junge Patienten bzw. Sportler mit einem erwarteten langfristigen Bedarf an einem ICD (ohne klinische Notwendigkeit für anti-bradykarde- bzw. antitachykarde Stimulationsfunktion) die idealen Kandidaten für eine S-ICD-Implantation (Tab. 2).
Kasuistik: 17 Jahre alter Basketballspieler mit Kardiomyopathie und rezidivierenden Synkopen
Nach jeweils nach körperlicher Anstrengung im Alltag aufgetretenen rezidivierenden Synkopen wurde bei einem 17-jährigen Nachwuchs-Bundesliga-Basketballspieler eine heriditäre hypertrophe Kardiomyopathie (HCM) diagnostiziert. Aus diesem Grund wurde die von der VBG/Basketdocs erarbeitete Eignung für die Teilnahme an der Nachwuchs-Basketball-Bundesliga (NBBL) vom Sportmediziner und Sportkardiologen mit dem Hinweis auf ein erhöhtes Arrhythmirisiko bei Wettkampfsport abgelehnt. Nach Bewertung der rezidivierenden Synkopen als überlebte arrhythmogene Ereignisse wurde die Indikation zur Implantation eines ICD getroffen und nach Abwägung der Vor- und Nachteile (u.a. Kontaktsport) die Entscheidung zur Implantation eines S-ICD getroffen und erfolgreich in unserem Zentrum durchgeführt (Abb. 1, 2 – 5). Als Konsequenz der nun gegebenen wirksamen Prävention eines arrhythmogenen plötzlichen Herztodes im Training und Wettkampf wurde anschließend die Eignung zur Teilnahme an der Nachwuchs-Basketball-Bundesliga (NBBL) erteilt, an der er nunmehr bereits seit sieben Monaten erfolgreich ohne subjektive Einschränkungen, nennenswerte Ereignisse, Folgeerscheinungen, unangemessene Schocks und ohne Elektroden- oder gerätebedingten Komplikationen, erfolgreich teilnimmt.
S-ICD: Der bessere ICD bei Sportlern mit arrhythmogenem Risiko
Aufgrund signifikant geringeren Elektroden-assoziierten Komplikationen sind S-ICD die bessere ICD-Behandlung bei jungen Patienten und insbesondere Sportlern mit einem erwarteten langfristigen Bedarf an einem ICD (ohne Notwendigkeit einer anti-bradykarden-/antitachykarden Stimulationsfunktion). Da die bei transvenöser Implantation häufig beobachteten Elektrodenkomplikationen (ca. 20 % während der ersten zehn Jahre; Tab. 1) Bewegungs- und Aktivitäts-assoziiert auftreten, sind S-ICD die ideale ICD-Therapie bei Sportlern mit erhöhtem arrhythmogenem Risiko bei zugrunde liegender struktureller oder elektrischer Herzerkrankung, auch um körperliche Aktivitäten und sogar die Teilnahme am Leistungssport einschließlich der damit verbundenen prognosewirksamen Effekten diesen Sportlern zu ermöglichen.
ICD und (Wettkampf-) Sport
Laut der European Association of Preventive Cardiology (EAPC) und der European Heart Rhythm Association (EHRA) wird körperliche Aktivität und sogar Leistungssport mit ICD empfohlen [25]. Die Registerdaten zeigten, dass Schocks bei körperlicher Aktivität in 10 – 20 % der Fälle und sogar häufiger während des Trainings (20 %) als im Wettkampf (10 %) auftreten [26]. Auch prominente Fußballspieler aus den höchsten europäischen Fußballligen (u. a. Antony van Loo, Belgien; Daley Blind, AJAX Amsterdam) haben wie Christian Eriksen (Dänemark) nach seinem arrhythmogenem Ereignis während der Fußball-EM 2021 einen TV-ICD implantiert. Katharina Bauer (Stabhochsprung) nahm erfolgreich mit S-ICD (wegen arrhythmogener Ereignisse) an den Olympischen Spielen 2021 in Tokio teil. Bei Sportlern mit ICD sind laut EAPC die 4-Ds (Danger, Disease, Device, Dysrhythmias) zu beachten: Danger…keine Gefahr für den ICD-Sportler und andere (z.B. Motorsport, Tauchen, Klettern). Disease… körperliche Aktivität mit ICD sollte kein Grund zur Verschlechterung der Grunderkrankung (disease) sein. Device… (z. B. kein Kampfsport oder Boxen), Kontaktsportarten (z. B. Fußball, Handball, Basketball) sollten mit externen Device/Geräteschutzmaßnahmen (z. B. Polsterung) durchgeführt werden. Dysrhythmias…sorgfältige ICD-Programmierung, um unangemessene Schocks zu vermeiden.
Literatur
[1] Zipes DP, Wellens HJ. Sudden Cardiac Death. Circulation 1998;98:2334 – 51
[2] Maron BJ , Roberts WC , McAllister HA , et al. Sudden death in young athletes. Circulation 1980;62:218–29
[3] Corrado D , Schmied C , Basso C , et al. Risk of sports: do we need a pre-participation screening for competitive and leisure athletes? Eur Heart J 2011;32:934–44
[4] Corrado D , Zorzi A. Sudden death in athletes. Int J Cardiol 2017;237:67–70
[5] Roberts WO, Stovitz SD. Incidence of sudden cardiac death in Minnesota high school athletes 1993-2012 screened with a standardized pre-participation evaluation. J Am Coll Cardiol 2013;62:1298–301
[6] Drezner JA, Rao AL, Heistand J, et al. Effectiveness of emergency response planning for sudden cardiac arrest in United States high schools with automated external defibrillators. Circulation 2009;120:518–25
[7] Harmon KG, Asif IM, Klossner D, et al. Incidence of sudden cardiac death in national collegiate athletic association athletes. Circulation 2011;123:1594–600.
[8] Drezner JA, Harmon KG, Marek JC. Incidence of sudden cardiac arrest in Minnesota high school student athletes: the limitations of catastrophic insurance claims. J Am Coll Cardiol 2014;63:1455–6.
[9] Egger F, Scharhag J, Kästner A, et al FIFA Sudden Death Registry (FIFA-SDR): a prospective, observational study of sudden death in worldwide football from 2014 to 2018 British Journal of Sports Medicine Published Online First: 23 December 2020. doi: 10.1136/bjsports-2020-102368.
[10] Massey A. Sudden Cardiac Arrest in Football. Sportaerztezeitung 2021, dec 11
[11] Moss AJ, HAll WJ, Cannom DS, et al. For the Multicenter Automatic Defibrillator Implantation Trial Investigators. Improved survival with an implanted defibrillator in patients with coronary disease at high risk for ventricular arrhythmia. N Engl J Med 1996;335:1933-40
[12] Connolly SJ, Hallstrom AP, Cappato R, et al. Meta-analysis of the implantable Cardioverter defibrillator secondary prevention trials. AVID, CASH and CIDS studies. Antiarrhythmics vs implantable defibrillator study. Cardiac arrest study Hamburg. Canadian Implantable defibrillator study. Eur Heart J 2000;21(24):2071-8
[13] Morrison TB, Rea RF, Hodge DO, Crusan D, Koestler C, Asirvatham SJ, Bradley D, Shen WK, Munger TM, Hammill SC, Friedman PA. Risk factors for implantable defibrillator lead fracture in a recalled and a nonrecalled lead. J Cardiovasc Electrophysiol. 2010 Jun 1;21(6):671-7. doi: 10.1111/j.1540-8167.2009.01683.x. Epub 2010 Jan 15. PMID: 20082653.
[14] Al-Ghamdi B. Subcutaneous Implantable Cardioverter Defibrillators: An Overview of Implantation Techniques and Clinical Outcomes. Curr Cardiol Rev. 2019;15(1):38-48. doi: 10.2174/1573403X14666180716164740. PMID: 30014805; PMCID: PMC6367695.
[15 Randles DA, Hawkins NM, Shaw M, Patwala AY, Pettit SJ, Wright DJ. How many patients fulfill the surface electrocardiogram criteria for subcutaneous implantable cardioverter-defibrillator implantation? Europe 2013;16:1015-21
[16] Burke MC, Gold MR, Knight BP, et al. Safety and efficacy of the totally subcutaneous implantable defibrillator: 2-years results from pooled analysis of the IDE study and EFFORTLESS registry. J Am Coll Cardiol 2015;65(16):1605-15
[17] Boersma L, Barr C, Knops R, et al. Implant and Midterm Outcomes of the Subcutaneous Implantable Cardioverter-Defibrillator Registry: The EFFORTLESS Study. J Am Coll Cardiol. 2017;70(7):830-841
[18] Weiss R, Knight BP, Gold MR, et al. Safety and Efficacy of a Totally Subcutaneous Implantable-Cardioverter Defibrillator. Circulation. 2013;128(9):944-953
[19] Knops RE, Olde Nordkamp LRA, Delnoy PHM, Boersma LVA, Kuschyk J, El-Chami MF, Bonnemeier H, Behr ER, Brouwer TF, Kääb S, Mittal S, Quast ABE, Smeding L, van der Stuijt W, de Weger A, de Wilde KC, Bijsterveld NR, Richter S, Brouwer MA, de Groot JR, Kooiman KM, Lambiase PD, Neuzil P, Vernooy K, Alings M, Betts TR, Bracke FALE, Burke MC, de Jong JSSG, Wright DJ, Tijssen JGP, Wilde AAM; PRAETORIAN Investigators. Subcutaneous or Transvenous Defibrillator Therapy. N Engl J Med. 2020 Aug 6;383(6):526-536. doi: 10.1056/NEJMoa1915932. PMID: 32757521.
[20] Steffel J. The subcutaneous ICD for prevention of sudden cardiac death: Current evidence and future directions. Pacing Clin Electrophysiol. 2020 Dec;43(12):1421-1427. doi: 10.1111/pace.14066. Epub 2020 Sep 17. PMID: 32896919.
[21] Lambiase PD, Barr C, Theuns DA, et al. EFFORTLESS Investigators: Worldwide experience with a totally subcutaneous implantable defibrillator. Early results from EFFORTLESS S-ICD Registry. Eur Heart J 2014;35:1657-65
[22] Kleemann T, Becker T, Doenges K, et al. Anaual reate of transvenous defibrillations lead defects in implantable cardioverter defibrillators over a period of >10 years. Circulation 2007;115:2474-80
[23] Moss AJ, Schurre C, Beck CA, et al. for the MADIT-RIT trial investigators. Reduction in inappropriate therapy and mortality through ICD programming. N Engl J Med 2012;367:2275-83
[24 Knops RE, Brouwer TF, Barr CS, et al. on behalf of the IDE and EFFORTLESS Investigators. The learning curve associated with the introduction of the subcutaneous implantable defibrillator. Europe 2016;18(7):101-5
[25] Pelliccia A, Solberg EE, Papadakis M, Adami PE, Biffi A, Caselli S, La Gerche A, Niebauer J, Pressler A, Schmied CM, Serratosa L, Halle M, Van Buuren F, Borjesson M, Carrè F, Panhuyzen-Goedkoop NM, Heidbuchel H, Olivotto I, Corrado D, Sinagra G, Sharma S. Recommendations for participation in competitive and leisure time sport in athletes with cardiomyopathies, myocarditis, and pericarditis: position statement of the Sport Cardiology Section of the European Association of Preventive Cardiology (EAPC). Eur Heart J. 2019 Jan 1;40(1):19-33. doi: 10.1093/eurheartj/ehy730. PMID: 30561613.
[26] Lampert R, Olshansky B, Heidbuchel H, Lawless C, Saarel E, Ackerman M, Calkins H, Estes NA, Link MS, Maron BJ, Marcus F, Scheinman M, Wilkoff BL, Zipes DP, Berul CI, Cheng A, Law I, Loomis M, Barth C, Brandt C, Dziura J, Li F, Cannom D. Safety of sports for athletes with implantable cardioverter-defibrillators: results of a prospective, multinational registry. Circulation. 2013 May 21;127(20):2021-30. doi: 10.1161/CIRCULATIONAHA.112.000447. PMID: 23690453.
Autoren
ist Facharzt für Innere Medizin mit Zusatzbezeichnungen Sportmedizin und Sportkardiologie und arbeitet im Herz- & Gefäßzentrum Göttingen. Zuvor war er stellv. und komm. Leiter der Abteilung für Kardiologie / Angiologie im Universitätsklinikum Greifswald. Außerdem ist er u.a. Mannschaftsarzt BG Göttingen (Basketball-BL, NBBL, JBBL).